2026-04-02
慢性神经痛(如糖尿病周围神经病变、三叉神经痛等)是一种折磨美国数百万人的顽疾。现有的小分子药物往往疗效不佳或伴随严重的脱靶副作用,而阿片类药物又极易导致成瘾。面对这一巨大的临床空白,基因治疗能否破局?
近期,顶级学术期刊《Science Translational Medicine》发表了由基因编辑先驱Sangamo Therapeutics团队主导的重磅临床前研究。研究团队利用AAV9载体递送工程化锌指阻遏蛋白(ZFRs),在小鼠及非人灵长类(NHP)模型中实现了对疼痛核心靶点Nav1.7的精准、长效且安全的抑制。这项研究不仅为慢性神经痛提供了全新的治疗范式,也标志着AAV基因治疗正加速向常见慢性病领域拓展。
1.屡战屡败的“完美靶点”:Nav1.7与小分子药物的困境
Nav1.7(由SCN9A基因编码)是痛觉信号传导的绝对核心,主要表达于外周初级伤害感受器中。人类遗传学为这一靶点提供了无懈可击的背书:SCN9A功能丧失突变会导致患者出现“先天性无痛症”,除了毫无痛觉,患者的运动、心血管及认知功能均完全正常;而其功能获得性突变则会引发红斑肢痛症等极度剧烈的慢性疼痛。
尽管靶点“完美”,成药之路却极其坎坷。由于Nav1.7与人体内其他Nav通道(如维持心脏跳动的Nav1.5和大脑功能的Nav1.1)在序列和结构上高度保守,传统小分子抑制剂极难做到绝对特异性。多种曾被寄予厚望的小分子药物在临床试验中因引发高血压、肝酶升高等严重脱靶副作用而宣告失败。因此,“如何只打Nav1.7,不误伤其他通道”成为了学界亟待解决的世纪难题。
2.另辟蹊径:ZFR联合AAV递送,不切DNA的表观遗传调控
面对特异性难题,Sangamo团队采用了其核心技术——工程化锌指阻遏蛋白(ZFRs)。相比于通过切割DNA引发双链断裂的CRISPR/Cas9系统,ZFRs展现出了独特的成药优势:
表观遗传级“调光器”:ZFR包含能够特异性识别 SCN9A 启动子区域的锌指阵列,以及一个KRAB抑制结构域。它通过空间占位和招募表观遗传修饰复合物,直接“关闭”基因转录,减少Nav1.7蛋白表达,全程不改变内源性基因组序列(图1A)。
低免疫原性与AAV高效包装:ZFR的核心组件源于人体天然蛋白,极大降低了免疫排斥风险。此外,ZFR序列短小紧凑,非常适合装载入腺相关病毒(如AAV6、AAV9)载体中,从而实现单次给药、长期起效的在体递送。
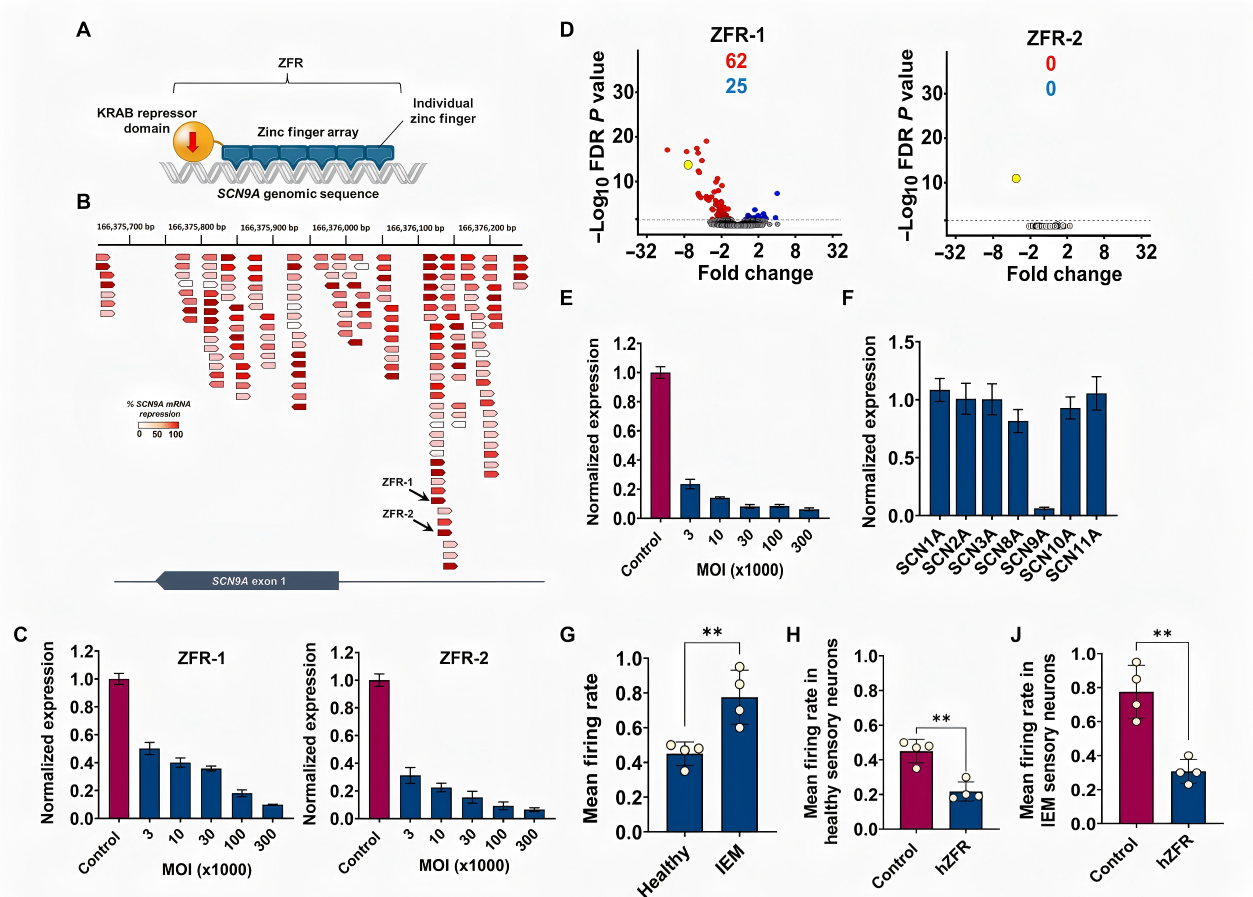
图1 体外实验中,靶向SCN9A的人源锌指重组酶(hZFR)可特异性下调人源SCN9A表达并抑制Nav1.7通道功能,且不影响诱导多能干细胞分化神经元中其他电压门控钠通道(Nav)的表达
(图片来源:Samie M et al, Sci Transl Med.,2026)
3.核心数据:从iPSC神经元到非人灵长类的全面验证
为验证这款基因药物的成药潜力,研究团队进行了严谨的转化医学评估:
体外极高的靶点特异性:在人类诱导多能干细胞(iPSC)衍生的神经元中,AAV6递送的人源ZFR(hZFR)精准且剂量依赖性地抑制了SCN9A(图1C, 1E)。微阵列转录组分析进一步证实了其惊人的特异性:hZFR仅下调了SCN9A,对全基因组超21000个基因(包括Nav1.6、Nav1.8等其他Nav家族成员)均无任何脱靶影响(图1D, 1F)。功能学验证显示,在源自致病突变患者的iPSC感觉神经元中,hZFR成功将热刺激诱发的高频神经放电降低了约两倍(图1G-1J)。
小鼠模型:强效逆转神经痛超敏反应在保留神经损伤(SNI)小鼠神经痛模型中,通过单次鞘内-腰椎(IT-L)注射AAV9-mZFR,小鼠背根神经节(DRG)中的靶基因表达量下降了约70%(图2F)。单细胞RNAscope原位杂交技术也证实了伤害感受器中Scn9a mRNA的大幅减少(图2G)。这一分子层面的抑制转化为显著的表型获益:治疗四周后,小鼠对机械刺激和冷刺激的疼痛阈值全面恢复至健康对照组水平(图3A, 3B)。同时,SmartCage动物行为分析表明,小鼠的夜间自发活动量和站立次数均显著改善,排除了药物导致运动迟缓的可能性(图3G, 3H)。
食蟹猴实验:支持临床转化的长期安全性基于前期的亮眼数据,团队将核心临床候选产品ST-503(AAV9递送,由神经元特异性Syn启动子驱动hZFR)推进至食蟹猴体内进行长达6个月的GLP毒理与药理评估。单次IT-L高剂量给药6个月后,猴子颈、胸、腰段DRG中的SCN9A表达量稳定维持在50%左右的抑制水平(图7B, 7C)。更为关键的是ST-503展现出的高安全性:猴子未表现出剂量限制性毒性,心电图、心率、血压以及各项生化指标均无异常(图7D, 8B)。神经传导速度(NCV)测试表明,外周运动和感觉神经功能完好无损(图8A)。组织病理学方面,仅在DRG等区域观察到了AAV基因治疗中常见的、且处于可接受范围内的轻微细胞浸润(图7E)。
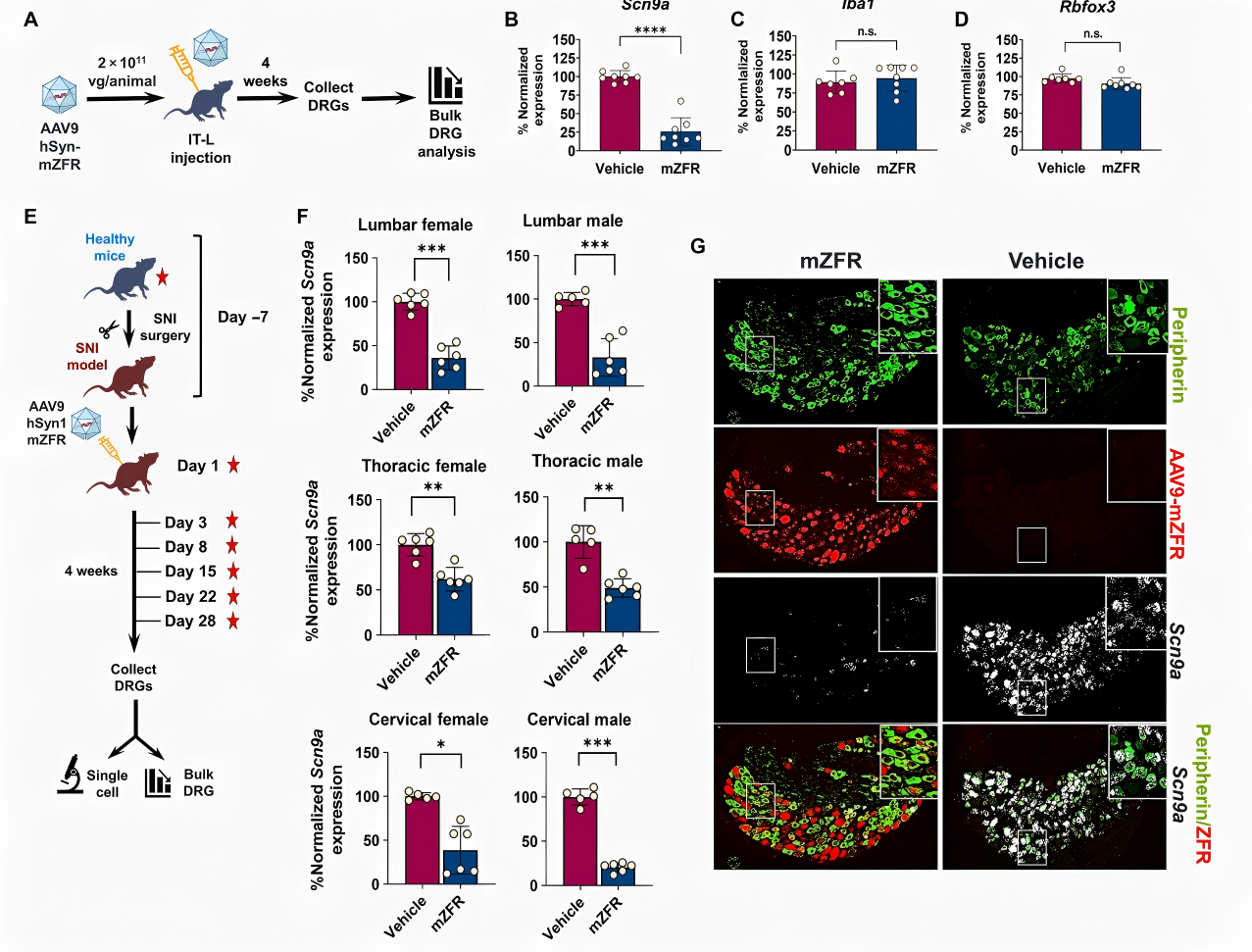
图2 ZFR介导的Scn9a基因抑制作用在神经病理性疼痛小鼠模型中的研究
(图片来源:Samie M et al, Sci Transl Med.,2026)
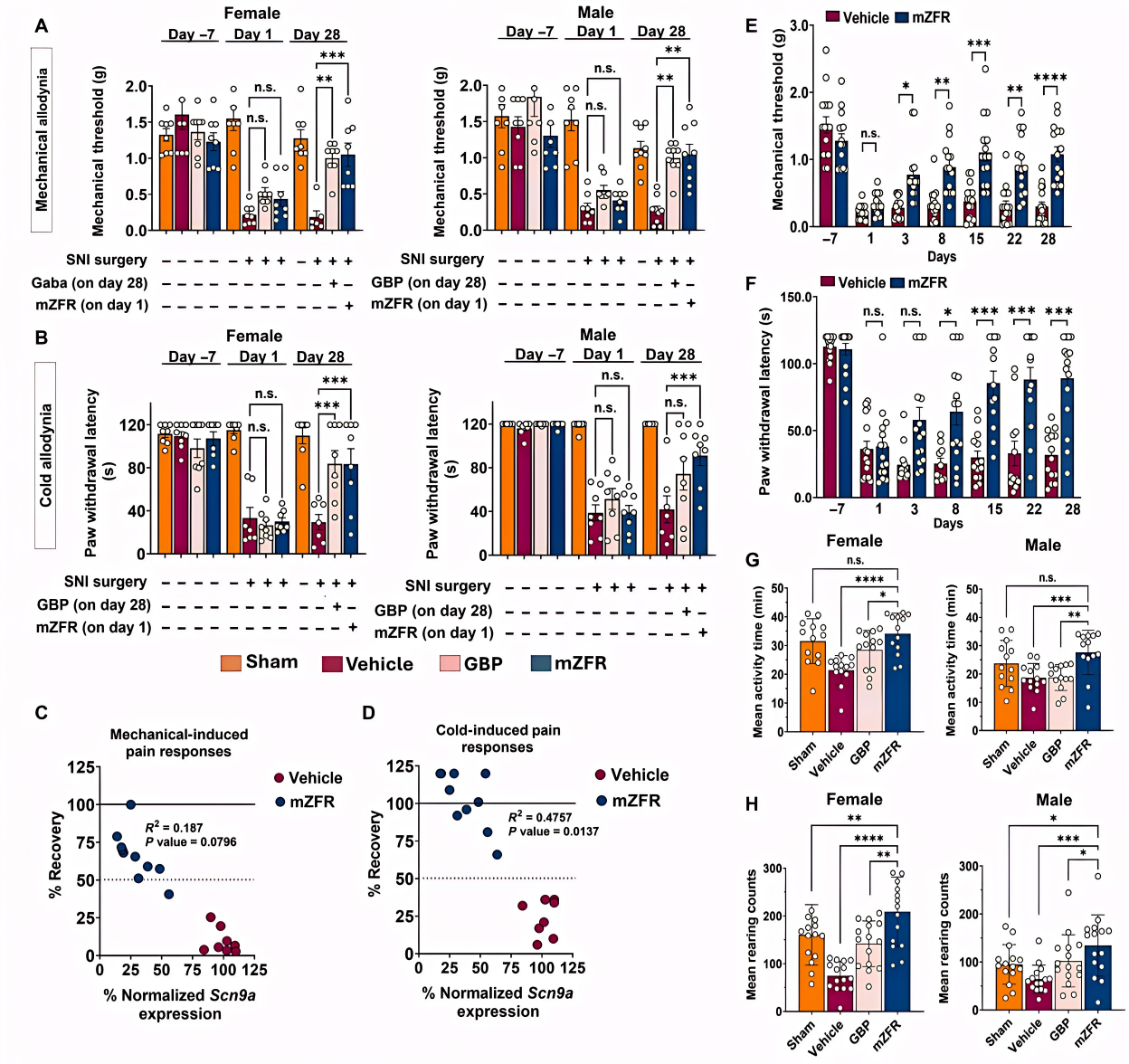 图3 在体抑制Scn9A可逆转神经病理性疼痛小鼠模型的痛觉过敏,且不影响小鼠整体自主活动水平
图3 在体抑制Scn9A可逆转神经病理性疼痛小鼠模型的痛觉过敏,且不影响小鼠整体自主活动水平
(图片来源:Samie M et al, Sci Transl Med.,2026)
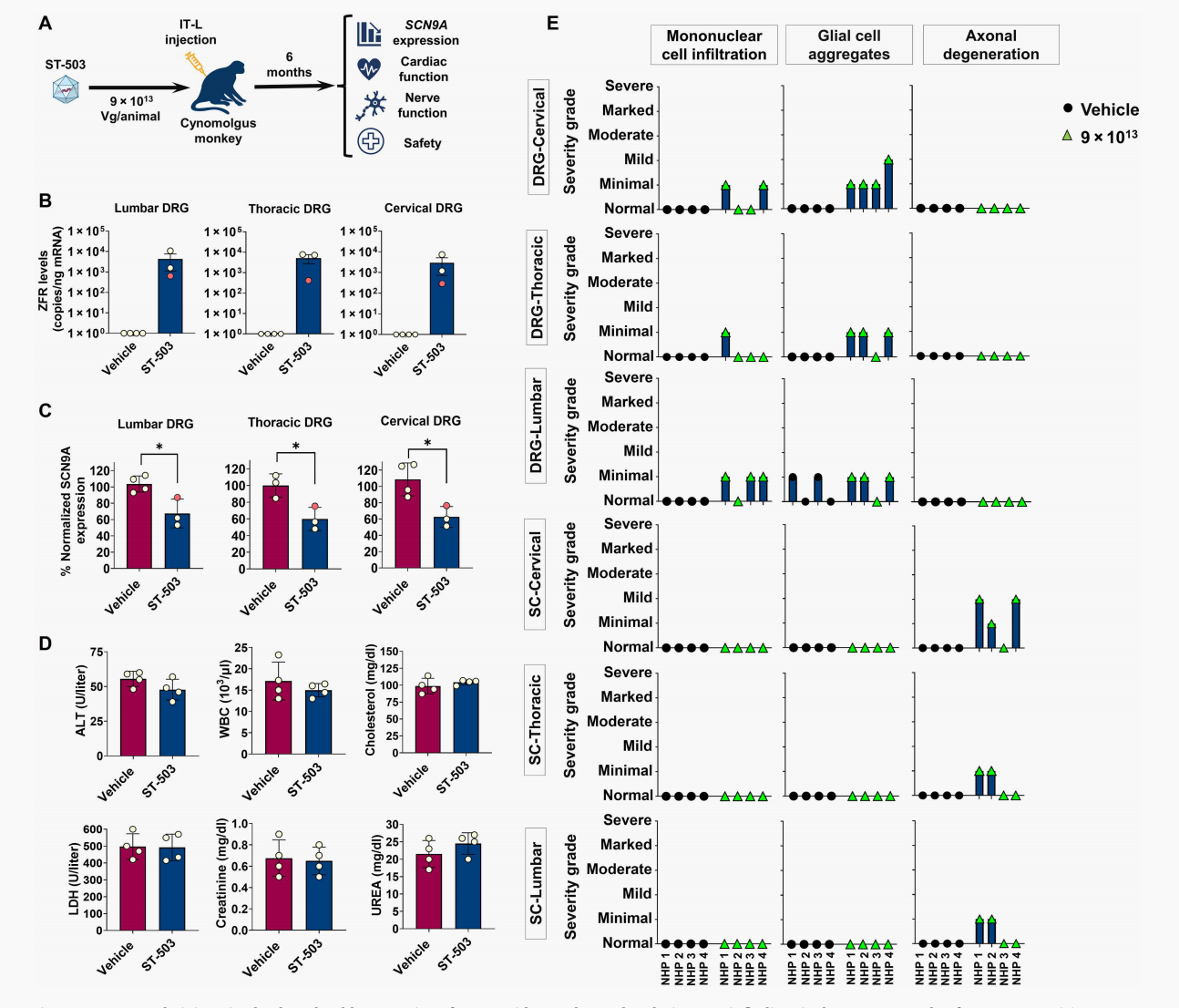
图7 经鞘内注射(IT-L)ST-503后,治疗6个月时可实现对SCN9A的长效抑制,并在背根神经节(DRG)中观察到与AAV载体类型相关的组织学显微表现
(图片来源:Samie M et al, Sci Transl Med.,2026)
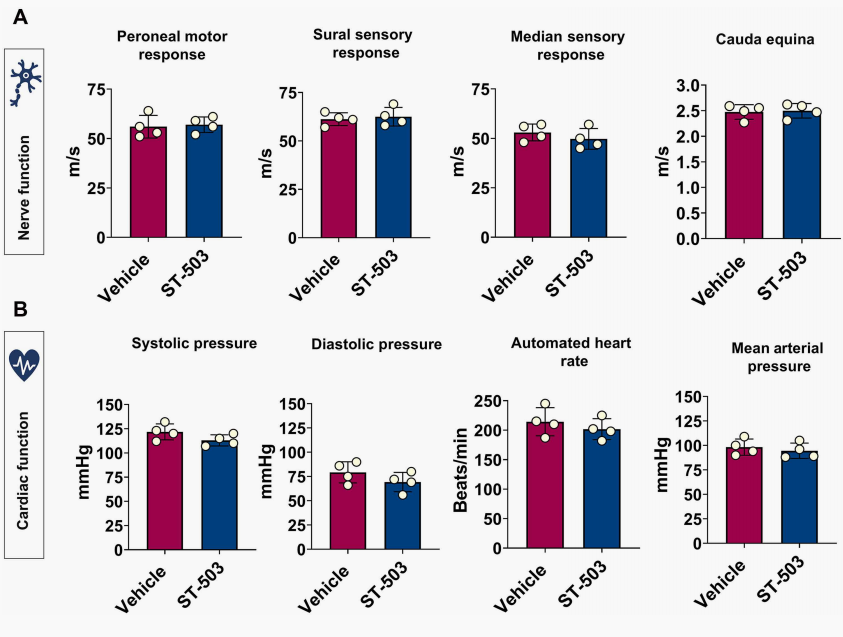
图8 在非人灵长类动物(NHP)中,经鞘内注射(IT-L)ST-503后6个月,未引起神经传导速度、心率或血压发生明显变化
(图片来源:Samie M et al, Sci Transl Med.,2026)
结语:AAV基因治疗进军常见慢性病的风向标
Sangamo团队的这项扎实研究证明了:工程化ZFR能够完美避开传统小分子药物的脱靶雷区,精准锚定Nav1.7靶点。单次AAV9鞘内给药即可实现长达半年的疾病修饰性获益,这对于目前需要长期忍受副作用、频繁服药的慢性神经痛患者而言,无疑具有颠覆性的临床价值。
目前,核心候选管线ST-503已展现出坚实的成药潜力,其针对特发性小纤维神经病患者的Ⅰ期临床试验(NCT06980948)也已在筹备中。如果临床转化顺利,我们或许将见证AAV基因治疗跨越罕见病边界,在更为广阔的常见慢性病市场中大放异彩。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。