2026-04-16
导读
嵌合抗原受体(CAR)-T细胞疗法早已改写了血液系统恶性肿瘤的治疗格局,但体外制备的复杂流程、有限的生产能力的临床局限,始终制约着其普及。2025年,《Nature Reviews Drug Discovery》发表的重磅综述:In vivo chimeric antigen receptor (CAR)-T cell therapy,聚焦“体内CAR-T细胞工程”这一颠覆性技术——无需体外操作,直接在患者体内生成CAR-T细胞,凭借病毒载体与脂质纳米颗粒(LNP)的技术突破,正在破解传统CAR-T的痛点,开启免疫治疗的全新赛道。本文将系统梳理这一领域的核心进展、主流技术平台、临床突破与未来展望,为科研从业者、临床医生及关注免疫治疗的读者,呈现最前沿的行业全景。
一、引言:从体外到体内,CAR-T疗法的必然转折
过去三十年,免疫治疗领域迎来爆发式发展,从单克隆抗体到免疫细胞衔接器,从DNA疫苗到RNA疫苗,每一项技术突破都在推动疾病治疗的革新。其中,体外CAR-T细胞疗法无疑是最具里程碑意义的成果之一——通过采集患者自身T细胞,体外基因修饰表达CAR后回输,在多种B细胞恶性肿瘤中展现出治愈潜力,成为无数复发/难治性患者的“最后希望”。
然而,尽管临床疗效显著,传统体外CAR-T疗法的推广速度却远不及预期,三大核心痛点成为其普及的“绊脚石”:一是制备与物流体系复杂,自体CAR-T需为每位患者单独制备,流程繁琐、耗时漫长,且对储存、运输条件要求极高;二是生产能力有限,全球合格的CAR-T生产基地稀缺,难以满足庞大的患者需求;三是依赖化疗清淋预处理,这类药物本身具有显著毒性,叠加CAR-T激活引发的不良反应,使得治疗仅能在具备资质的大型医疗中心开展,进一步限制了患者可及性。
在此背景下,“体内CAR-T细胞工程”应运而生——无需体外分离、修饰T细胞,直接通过靶向递送系统,将编码CAR的遗传物质递送至患者体内的内源性T细胞,原位生成CAR-T细胞。这一策略不仅彻底消除了体外操作的繁琐流程,更有望规避化疗预处理的毒性,拓宽CAR-T疗法的适用范围,从血液肿瘤延伸至自身免疫性疾病等更多领域。2025年,随着多项技术进入临床阶段,体内CAR-T疗法已成为免疫治疗领域最受关注的研究热点,正在开启免疫治疗的“第二次革命”。
二、体外CAR-T的经验:为体内技术铺路,明确优化方向
截至目前,已有多款基于逆转录病毒或慢病毒载体的自体CAR-T产品获批,用于治疗B细胞急性淋巴细胞白血病、非霍奇金淋巴瘤、多发性骨髓瘤等疾病,全球超过1000项临床试验正在推进。这些体外CAR-T产品的临床实践,不仅证实了CAR技术的强效治疗潜力,更积累了大量宝贵经验,为体内CAR-T疗法的开发提供了重要指导。
1. CAR-T疗法的变革性价值:不止于肿瘤治疗
体外CAR-T疗法的核心价值,在于其“治愈性”潜力——在部分血液肿瘤患者中,CAR-T治疗可实现持久缓解,甚至达到临床治愈。更令人惊喜的是,其应用范围正在不断拓展,从肿瘤领域延伸至自身免疫性疾病。临床前研究与多项临床案例显示,CAR-T疗法可通过“免疫重置”机制,清除自身反应性记忆B细胞,降低疾病相关生物标志物水平,在狼疮性肾炎、肌炎、系统性硬化症等自身免疫性疾病中,实现持久、无需药物维持的缓解。
这种“免疫重置”,本质上是将包含致病性自身反应性免疫细胞的免疫组库,替换为功能正常的免疫系统,其效果类似于大剂量化疗后自体干细胞移植,但无需复杂的干细胞采集与回输流程,安全性更具优势。此外,体外CAR-T产品的大规模临床应用,也推动了治疗相关不良事件的分级与管理体系的标准化,包括细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性(ICANS)等,为体内CAR-T疗法的临床安全管理提供了重要参考。
2. 体外CAR-T的局限性:催生体内技术的创新需求
尽管成就显著,体外CAR-T疗法的局限性依然突出,主要集中在三个方面:
一是可及性极低。由于自体CAR-T需个体化制备,且依赖复杂的生产工艺与物流体系,美国约五分之四符合条件的淋巴瘤患者无法获得商业化CAR-T产品,全球范围内的可及性差距更为明显。高昂的生产成本,也使得这类疗法难以向低收入人群普及。
二是安全性门槛高。化疗清淋预处理是体外CAR-T治疗的常规步骤,其目的是为回输的CAR-T细胞创造扩增空间,但烷化剂、嘌呤类似物等预处理药物会带来骨髓抑制、感染等毒性,叠加CAR-T激活引发的CRS、ICANS等不良反应,使得治疗需在具备重症监护能力的医疗中心开展,限制了其在基层医院的应用。
三是疗效存在瓶颈。部分患者对CAR-T治疗无响应或出现耐药,核心原因包括免疫细胞健康状态不佳、肿瘤微环境的免疫抑制作用,以及靶抗原低表达或异质性表达导致的免疫逃逸。这些问题,仅通过优化体外制备流程难以彻底解决,亟需全新的技术策略。
正是这些局限性,推动了CAR-T疗法从“体外”向“体内”的转型——体内CAR-T无需体外操作与化疗预处理,不仅能大幅提升可及性、降低成本,更有望通过原位工程化,调动更广泛的免疫机制,突破体外CAR-T的疗效瓶颈。
三、体内CAR-T的发展历程:从实验室突破到产业爆发
体内CAR-T疗法的诞生,是纳米技术、RNA药物、病毒学与CAR技术交叉融合的结果。这一领域的发展,大致可分为三个阶段:实验室突破、产业布局、临床转化,每一个阶段都伴随着关键技术的革新。
2017年8月,Fred Hutchinson癌症中心的Matthias Stephan团队首次报道了体内CAR-T的临床前突破:他们开发了可生物降解、携带DNA的聚合物纳米颗粒,靶向小鼠T细胞表面的CD3分子,递送编码CD19特异性CAR的基因负载。在急性淋巴细胞白血病小鼠模型中,静脉输注该纳米颗粒后,原位生成的CAR-T细胞展现出与体外CAR-T相当的抗肿瘤效果,且无需体外细胞操作,首次证实了体内CAR-T的可行性。
2018年9月,Paul-Ehrlich研究所的Christian Buchholz团队进一步推进了这一技术,他们开发了人CD8靶向慢病毒载体,在人源化小鼠模型中实现了T细胞的原位工程化,伴随B细胞清除与细胞因子产生,为病毒载体用于体内CAR-T奠定了基础。
尽管实验室突破令人振奋,但体内CAR-T的产业转化在初期却进展缓慢,主要原因有三点:一是这些突破未被当时的风险投资与生物制药行业广泛关注;二是Novartis、Kite等企业的体外CAR-T产品刚刚获批,市场对体外技术的信心更高;三是体内CAR-T依赖的纳米药物递送技术,当时尚未被主流生物制药企业熟悉,开发风险被认为高于体外技术。
转折点出现在2018年7月,首家专注于体内CAR-T疗法的生物技术公司Tidal Therapeutics成立,随后Umoja Biopharma、Orna Therapeutics、Sana Biotechnology等企业相继诞生,开启了体内CAR-T的产业布局热潮。2021年以来,大型生物制药企业纷纷入局:Sanofi收购Tidal Therapeutics,Astra Zeneca收购EsoBiotec,Abbvie收购Capstan Therapeutics,截至2025年,全球已有超过30家企业参与体内CAR-T的研发,形成了多元化的产业生态。
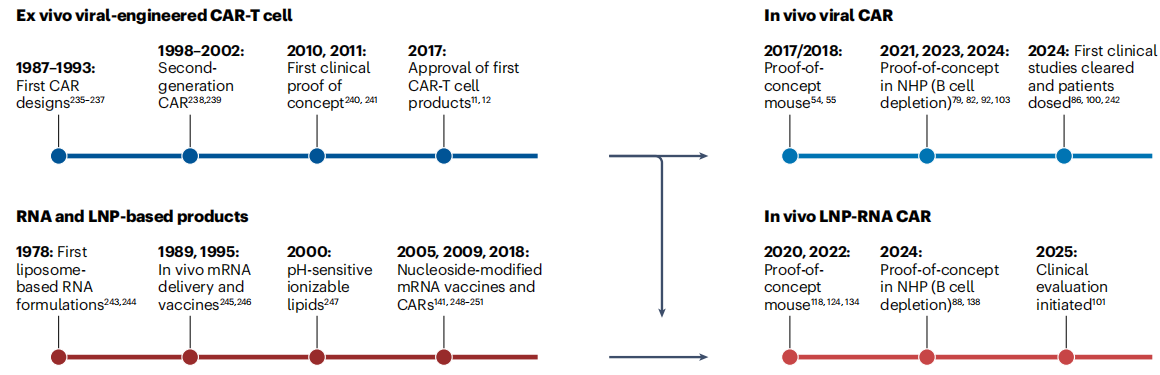
图1 推动体内CAR技术临床转化的重大发现与里程碑事件
(图片来源:Bot A et al, Nat Rev Drug Discov., 2026)
四、体内CAR-T的核心机制:原位工程化,无需体外操作与预处理
体内CAR-T的核心优势,在于“原位工程化”——通过现货型载体或制剂,直接对患者体内的免疫细胞进行基因修饰,生成CAR-T细胞,无需体外分离、培养与回输,也无需化疗清淋预处理。这一机制,不仅简化了治疗流程,更带来了独特的药理优势。
与体外CAR-T不同,体内CAR-T的治疗流程极为简便:患者仅需静脉输注携带CAR基因负载的递送载体(病毒载体或LNP),载体将自动靶向体内的T细胞(或其他免疫细胞),将CAR基因递送至细胞内,实现CAR的表达,进而激活T细胞,清除靶细胞。由于无需清淋预处理,患者体内的免疫细胞得以保留,不仅降低了治疗毒性,还能调动天然免疫系统的协同作用,增强治疗效果。
要实现高效的原位工程化,递送载体必须具备两个核心特征:一是卓越的细胞选择性,能够精准靶向T细胞(或其他目标免疫细胞),避免被非目标细胞摄取,降低脱靶毒性;二是高效的基因递送能力,能够将CAR基因高效递送至细胞内,实现CAR的稳定或瞬时表达。
目前,进入临床开发的体内CAR-T平台,主要分为两大类,基于不同的基因负载与递送策略,各有优势:
第一类是“整合型平台”,以工程化慢病毒载体为核心,将CAR基因整合到T细胞的基因组中,实现CAR的持久表达。这类平台的优势的是,CAR-T细胞可根据靶抗原的存在与负荷,自我调节扩增与存续状态,适合需要长期CAR活性的疾病,如晚期肿瘤。
第二类是“瞬时表达平台”,以LNP递送RNA为核心,CAR基因以线性或环状RNA的形式存在,不整合到细胞基因组中,实现CAR的瞬时表达。这类平台的优势是,CAR表达可通过调整给药剂量与频率进行调控,安全性更高,适合对安全性要求高的适应症,如自身免疫性疾病。
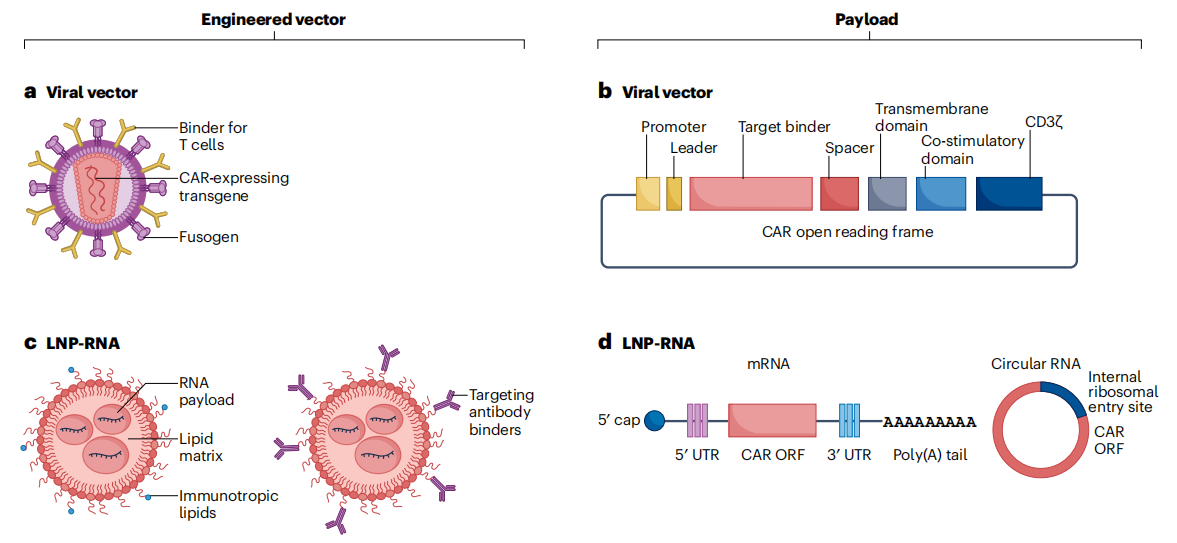
图2 主要体内CAR平台(重点关注工程载体及治疗载荷)
(图片来源:Bot A et al, Nat Rev Drug Discov., 2026)
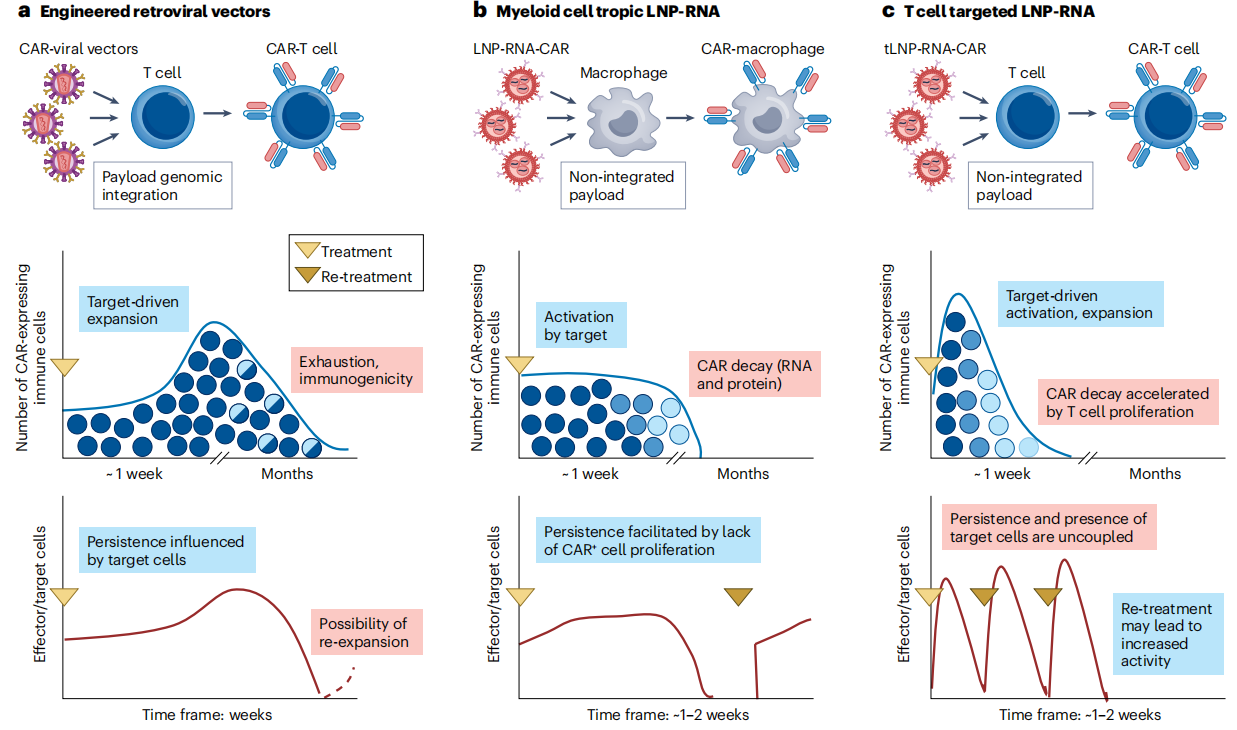
图3 处于研发阶段的主要体内CAR平台及其作用机制
(图片来源:Bot A et al, Nat Rev Drug Discov., 2026)
五、主流技术平台:病毒载体 VS RNA-LNP,各领风骚
2025年,体内CAR-T的研发格局已基本清晰,病毒载体与RNA-LNP两大平台并驾齐驱,各自凭借独特的技术优势,占据不同的研发赛道。以下将详细梳理两大平台的核心技术、代表企业与临床进展,呈现体内CAR-T的技术全景。
1.病毒载体平台:持久表达,聚焦肿瘤治疗
病毒载体平台的核心是工程化慢病毒(或γ逆转录病毒)载体,通过改造病毒包膜蛋白,实现对T细胞的特异性靶向,将CAR基因整合到T细胞基因组中,实现CAR的持久表达。这类平台的关键技术突破,在于病毒包膜的工程化改造——消除病毒与天然细胞表面受体的相互作用,同时展示识别T细胞特异性标志物(如CD3、CD8、CD7)的高亲和力结合域,确保精准靶向T细胞。
目前,用于体内CAR-T的病毒包膜蛋白主要包括麻疹病毒糖蛋白、尼帕病毒(NiV)糖蛋白、水疱性口炎病毒(VSV)G糖蛋白等,其中NiV糖蛋白与VSV-G糖蛋白因转导效率高、安全性好,成为最常用的包膜蛋白。此外,通过在病毒包膜上整合CD47等“别吃我”信号,可避免载体被巨噬细胞清除,进一步提升转导效率。
截至2025年,已有多家企业的病毒载体类体内CAR-T产品进入临床阶段,代表企业与核心进展如下:
(1)Interius BioTherapeutics(吉利德旗下)
该公司开发的工程化慢病毒载体,通过Gen 2.1融合蛋白(VSV-G蛋白的改造版本)进行假型化,降低脱靶结合并提升血液稳定性,同时通过CD7特异性结合域,实现对T细胞与NK细胞的特异性靶向。其核心候选产品INT2104,是一种CD7靶向慢病毒载体,递送抗CD20 CAR,用于治疗B细胞恶性肿瘤。
临床前研究显示,INT2104在非人灵长类(NHP)与小鼠模型中,可实现T细胞与NK细胞的特异性转导,生成功能性抗CD20 CAR细胞,有效清除CD20+ B细胞,且耐受性良好,无CRS与神经毒性。2024年10月,INT2104的I期临床试验(NCT06539338)完成首例患者给药,评估其治疗复发/难治性B细胞恶性肿瘤的安全性,数据预计于2025年下半年公布。此外,该公司还在开发INT2106(抗CD19 CAR),用于自身免疫性疾病的治疗。
(2)Umoja Biopharma(艾伯维合作)
该公司的VivoVec平台,是一种表面工程化的第三代慢病毒载体,使用Cocal融合病毒糖蛋白进行假型化,对人血清灭活具有抗性,提升体内稳定性。同时,载体表面整合了抗CD3 scFv、CD80与CD58共刺激配体,既实现对T细胞的特异性靶向,又能激活T细胞,模拟抗原呈递细胞的功能。
其核心产品UB-VV111,编码CD19靶向CAR与雷帕霉素激活细胞因子受体(RACR),可在体内生成共表达RACR系统的CD19 CAR-T细胞,实现雷帕霉素诱导的CAR-T细胞扩增与生存能力提升。2024年7月,UB-VV111获得FDA IND批准,启动I期临床试验,治疗B细胞恶性肿瘤。NHP模型显示,单次输注后,CAR-T细胞峰值可达循环T细胞的65%,实现快速且持久的B细胞清除,炎症不良事件可通过标准免疫抑制治疗控制。此外,该公司还在开发UB-VV400(抗CD22 CAR),聚焦B细胞恶性肿瘤与自身免疫性疾病。
(3)EsoBiotec(阿斯利康旗下)
该公司的技术平台基于第三代自失活、VSV-G蛋白靶向缺陷型慢病毒载体,通过靶向TCRαβ的特异性结合域,实现T细胞的精准靶向,同时通过MHC I类分子敲除与CD47表达,实现免疫学隐身,降低载体被免疫系统清除的风险。其核心产品为抗BCMA CAR,用于治疗多发性骨髓瘤。
临床前研究显示,该产品可有效工程化静息与活化T细胞,在多发性骨髓瘤模型中实现肿瘤清除。近期报道的首例接受该产品治疗的多发性骨髓瘤患者,在治疗第28天即获得客观缓解,骨髓中播散性病灶被清除,凸显了其快速起效的优势。目前,已有4例多发性骨髓瘤患者获得客观缓解,良好的疗效与安全性,推动了阿斯利康对EsoBiotec的收购。
(4)其他代表性企业
Kelonia Therapeutics的iGPS平台,通过抗CD3单链抗体与去靶向VSV-G结合,实现对T细胞的高特异性靶向,其核心产品KLN-1010(抗BCMA CAR)在临床前模型中,疗效优于商业化体外CAR-T产品,计划于2025年进入临床。Sana Biotechnology的靶向融合素平台,使用副黏病毒来源的融合素,实现T细胞的精准转导,避免内体途径带来的脱靶摄取,目前正在推进抗CD19 CAR产品的临床开发。此外,深圳金古瑞的抗CD3修饰逆转录病毒载体,已在研究者发起试验中,实现了复发/难治性弥漫大B细胞淋巴瘤患者的部分缓解,为国内体内CAR-T的研发提供了重要参考。
2. RNA-LNP平台:瞬时可调,兼顾肿瘤与自身免疫
RNA-LNP平台的核心,是通过脂质纳米颗粒(LNP),将编码CAR的线性或环状RNA递送至目标免疫细胞,实现CAR的瞬时表达。这类平台的崛起,得益于COVID-19疫情期间mRNA疫苗与LNP制剂的技术突破——可电离脂质的创新,使得LNP具备高生物可降解性与低免疫原性,支持重复给药,同时通过抗体功能化或免疫嗜性设计,实现对T细胞或髓系细胞的特异性靶向。
与病毒载体平台相比,RNA-LNP平台的优势在于:无需基因整合,安全性更高;CAR表达瞬时可控,可通过重复给药调整暴露水平,适合对安全性要求高的适应症;生产工艺相对简单,成本更低,更易实现规模化生产。目前,RNA-LNP平台主要分为两类:一类是靶向T细胞的tLNP(靶向LNP),用于生成CAR-T细胞;另一类是利用LNP的髓系细胞嗜性,靶向巨噬细胞,生成CAR-巨噬细胞(CAR-M),聚焦实体瘤治疗。
截至2025年,已有多家企业的RNA-LNP类体内CAR-T产品进入临床阶段,代表企业与核心进展如下:
(1)Myeloid Therapeutics
该公司是体内CAR-M领域的领军企业,利用LNP的天然髓系细胞嗜性,将CAR mRNA递送至巨噬细胞,实现CAR-M的原位生成。其CAR设计包含截短FcαR(CD89)融合结构,与内源性FcRγ链形成复合物,确保CAR在巨噬细胞表面的稳定表达与功能激活。同时,通过优化mRNA序列与3’非翻译区(UTR),延长CAR表达时间。
该公司已有两款候选产品进入I期临床试验:MT-302(靶向TROP2)用于治疗TROP2+上皮恶性肿瘤,MT-303(靶向GPC3)用于治疗肝细胞癌。临床数据显示,MT-302可在患者外周血与肿瘤微环境中实现CAR表达,MT-303在多线治疗失败的肝细胞癌患者中展现出抗肿瘤活性,病灶缩小,且耐受性良好,未观察到剂量限制性毒性,CRS可控。此外,该公司还在开发抗HER2 CAR-M,聚焦实体瘤治疗。
(2)Capstan Therapeutics(艾伯维旗下)
该公司的CellSeeker技术平台,通过抗体修饰的tLNP,实现对T细胞亚群的选择性靶向,递送优化的线性mRNA CAR负载。其tLNP包含高度生物可降解的可电离脂质,免疫原性低,支持重复静脉输注,适合长期治疗。
核心候选产品为抗CD19 CAR,靶向CD8+ T细胞,用于自身免疫性疾病的治疗。临床前研究显示,该产品可在人源化小鼠模型中快速实现CD8+ T细胞的原位工程化,有效清除恶性B细胞;在NHP模型中,两次输注即可实现淋巴器官与骨髓中B细胞的深度清除,随后以初始B细胞为主重建,实现“免疫重置”,为自身免疫性疾病的治疗提供了新路径。2025年,该产品的I期临床试验(NCT06917742)已启动,评估其治疗系统性红斑狼疮等自身免疫性疾病的安全性与疗效。
(3)深圳MagicRNA
该公司的Enc-LNP平台,包含专有抗体片段与可电离脂质,可选择性靶向CD8+ T细胞,递送抗CD19 CAR mRNA。其核心产品HN2301,正在开展研究者发起试验,治疗复发/难治性系统性红斑狼疮患者。临床前研究显示,HN2301在狼疮肾炎小鼠模型中具有显著活性,在NHP模型中实现了B细胞的深度清除与免疫重置。截至2025年,该试验已展现出体内工程化抗CD19 CAR-T细胞的首个证据,伴随B细胞清除、细胞因子产生,以及患者自身抗体滴度的下降,验证了平台的可行性。
(4)其他代表性企业
Orna Therapeutics的独特之处,在于使用免疫嗜性脂质配制的LNP,无需抗体修饰即可优先靶向免疫细胞,同时使用环状RNA作为CAR负载,延长CAR表达时间。临床前研究显示,其抗CD20 CAR制剂在NHP中可实现95%的血液B细胞清除,计划于2026年前启动I期临床试验,聚焦自身免疫性疾病与血液肿瘤。赛诺菲(Sanofi)也在开发tLNP平台,通过抗CD8抗体修饰LNP,靶向CD8+ T细胞,递送mRNA CAR,临床前研究显示可实现快速CAR表达,无脱靶激活,计划推进至临床开发。此外,Carisma与Moderna合作开发的CAR-M平台,靶向GPC3,用于肝细胞癌治疗,目前处于临床前阶段,临床前数据显示其在荷瘤小鼠模型中具有强效抗肿瘤活性。
六、临床进展:从概念验证到初步疗效,曙光初现
截至2025年,体内CAR-T疗法已进入临床探索的关键阶段,首批进入临床的候选产品,主要聚焦于血液肿瘤与实体瘤,初步数据展现出良好的安全性与抗肿瘤活性,为后续开发奠定了坚实基础。
在血液肿瘤领域,病毒载体类产品表现突出:EsoBiotec的抗BCMA CAR产品,在4例多发性骨髓瘤患者中实现客观缓解,其中1例在治疗第28天达到严格完全缓解(sCR),另1例实现骨髓微小残留病(MRD)清除,凸显了体内CAR-T快速起效的优势;深圳金古瑞的抗CD19 CAR产品,在复发/难治性弥漫大B细胞淋巴瘤患者中,实现部分缓解,治疗后3个月达到完全缓解,且不良反应轻微,仅出现1级CRS与骨髓毒性,无神经毒性。
在实体瘤领域,RNA-LNP类产品展现出独特优势:Myeloid Therapeutics的MT-303(靶向GPC3),在多线治疗失败的肝细胞癌患者中,实现病灶缩小,验证了CAR-M在实体瘤中的治疗潜力;MT-302(靶向TROP2)在TROP2+实体瘤患者中,实现CAR在肿瘤微环境中的表达,为实体瘤的治疗提供了新方向。
安全性方面,目前已公布的临床数据显示,体内CAR-T疗法的耐受性良好,未出现严重不良事件或剂量限制性毒性。病毒载体类产品的CRS呈现双相特征,第一个峰值出现在输注后数小时,与载体输注反应相关,第二个峰值出现在治疗后7-14天,与CAR-T细胞扩增相关,均可控;RNA-LNP类产品未出现明显的肝脏毒性与超敏反应,重复给药的耐受性良好。
需要注意的是,目前体内CAR-T的临床研究仍处于早期阶段,大多数试验采用低起始剂量、缓慢剂量递增的策略,同时加强患者监测,以确保安全性。随着临床数据的不断积累,给药方案将进一步优化,疗效也有望进一步提升。此外,体内CAR-T在自身免疫性疾病中的临床探索,也已取得初步进展,深圳魔RNA的HN2301在系统性红斑狼疮患者中,实现了自身抗体滴度的下降,为自身免疫性疾病的治疗开辟了新路径。
表1 基于慢病毒的体内CAR-T细胞技术平台(研发阶段)
(表格来源:Bot A et al, Nat Rev Drug Discov., 2026)
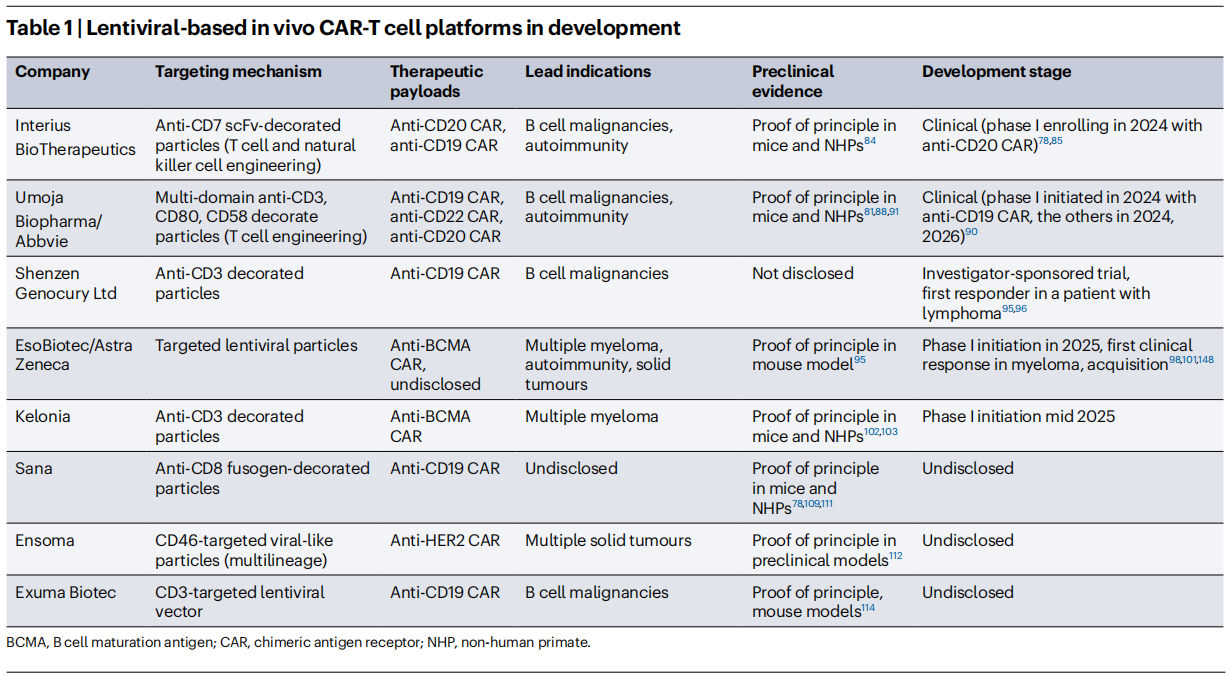
表2 基于脂质纳米颗粒(LNP)-RNA的体内CAR-T细胞技术平台(研发阶段)
(表格来源:Bot A et al, Nat Rev Drug Discov., 2026)
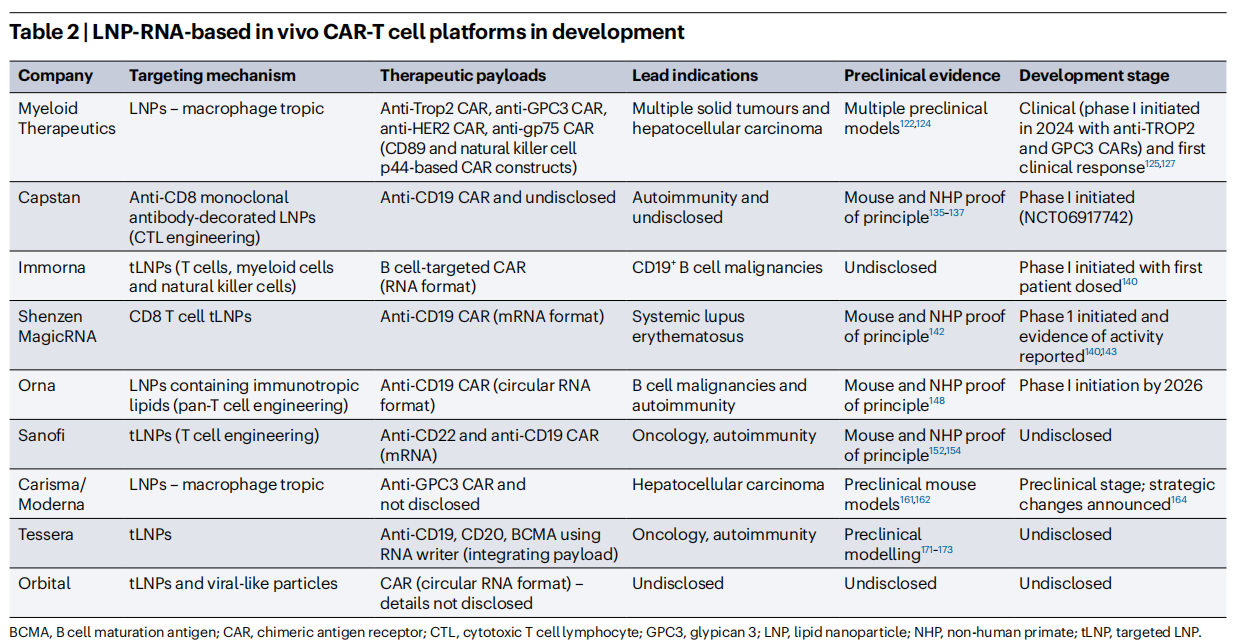
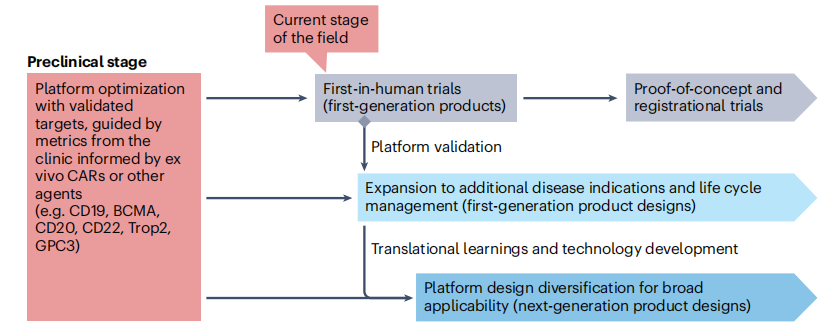
图4 体内CAR疗法的发展总览与前沿展望
(图片来源:Bot A et al, Nat Rev Drug Discov., 2026)
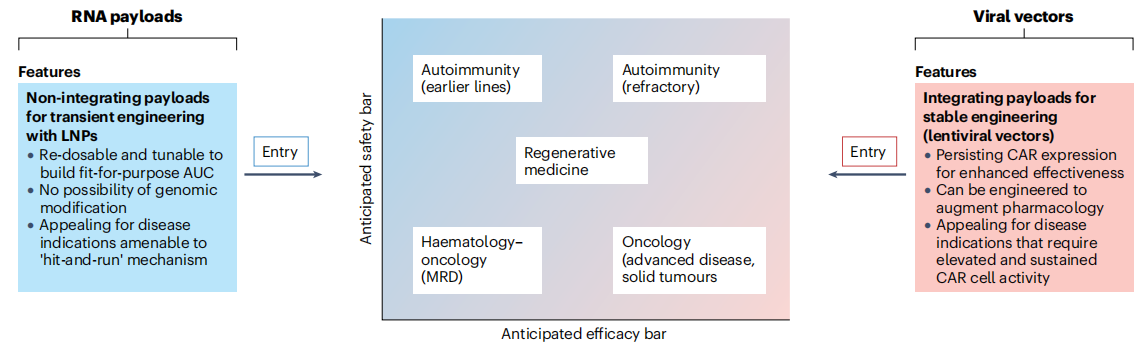
图5 体内工程平台的特性为目标产品谱特征及治疗适用性提供参考
(图片来源:Bot A et al, Nat Rev Drug Discov., 2026)
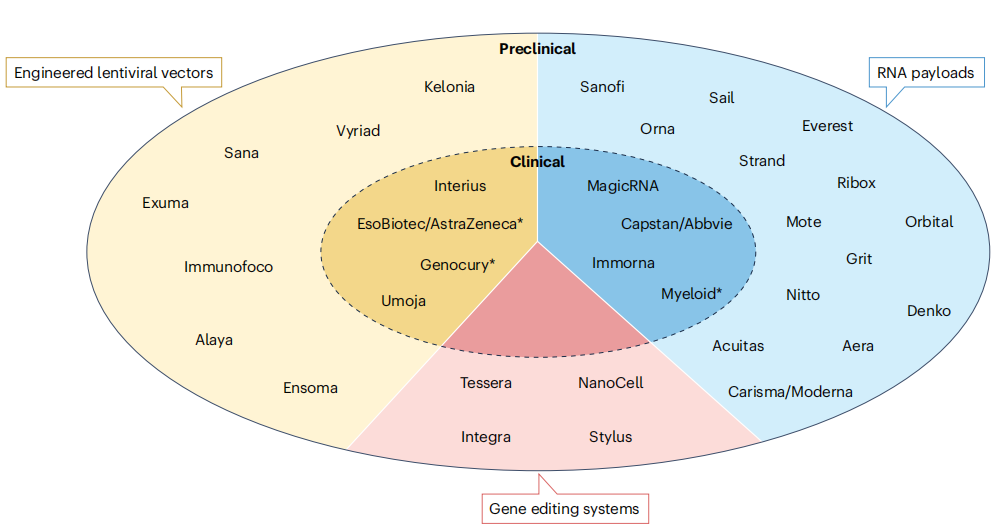
图6 快速发展的体内CAR疗法生态系统
(图片来源:Bot A et al, Nat Rev Drug Discov., 2026)
七、未来展望:重新定义免疫治疗,惠及更多患者
从1990年首次以质粒DNA进行体内基因免疫接种,到1999年首次静脉输注逆转录病毒载体用于临床治疗,再到2017年首个CAR-T产品获批,免疫治疗的每一步突破,都在推动医学的进步。2025年,体内CAR-T疗法的临床探索,标志着免疫治疗进入了“精准编程”的新时代——无需体外操作,无需化疗预处理,通过现货型制剂,即可实现免疫系统的原位工程化,为更多患者带来希望。
未来,体内CAR-T疗法的发展,将聚焦于三个核心方向:一是技术优化,通过病毒包膜与LNP的设计革新,提升靶向性与递送效率,解决CAR表达的持久性与瞬时性平衡问题;二是适应症拓展,从血液肿瘤与自身免疫性疾病,延伸至实体瘤、再生医学、感染性疾病等领域,实现“一药多治”;三是产业化升级,优化生产工艺,降低生产成本,推动体内CAR-T疗法的规模化生产,提升可及性,让更多低收入患者能够负担得起。
我们有理由相信,随着技术的不断突破与临床数据的不断积累,体内CAR-T疗法将彻底改变免疫治疗的格局——它不仅能突破体外CAR-T的可及性瓶颈,更能凭借精准的靶向性、良好的安全性,在更广泛的疾病中实现治愈潜力。在CAR-T疗法诞生8年后的今天,体内CAR-T正在重新定义免疫治疗的未来,有望成为继PD-1/PD-L1抑制剂之后,又一款改变疾病治疗结局的革命性疗法。
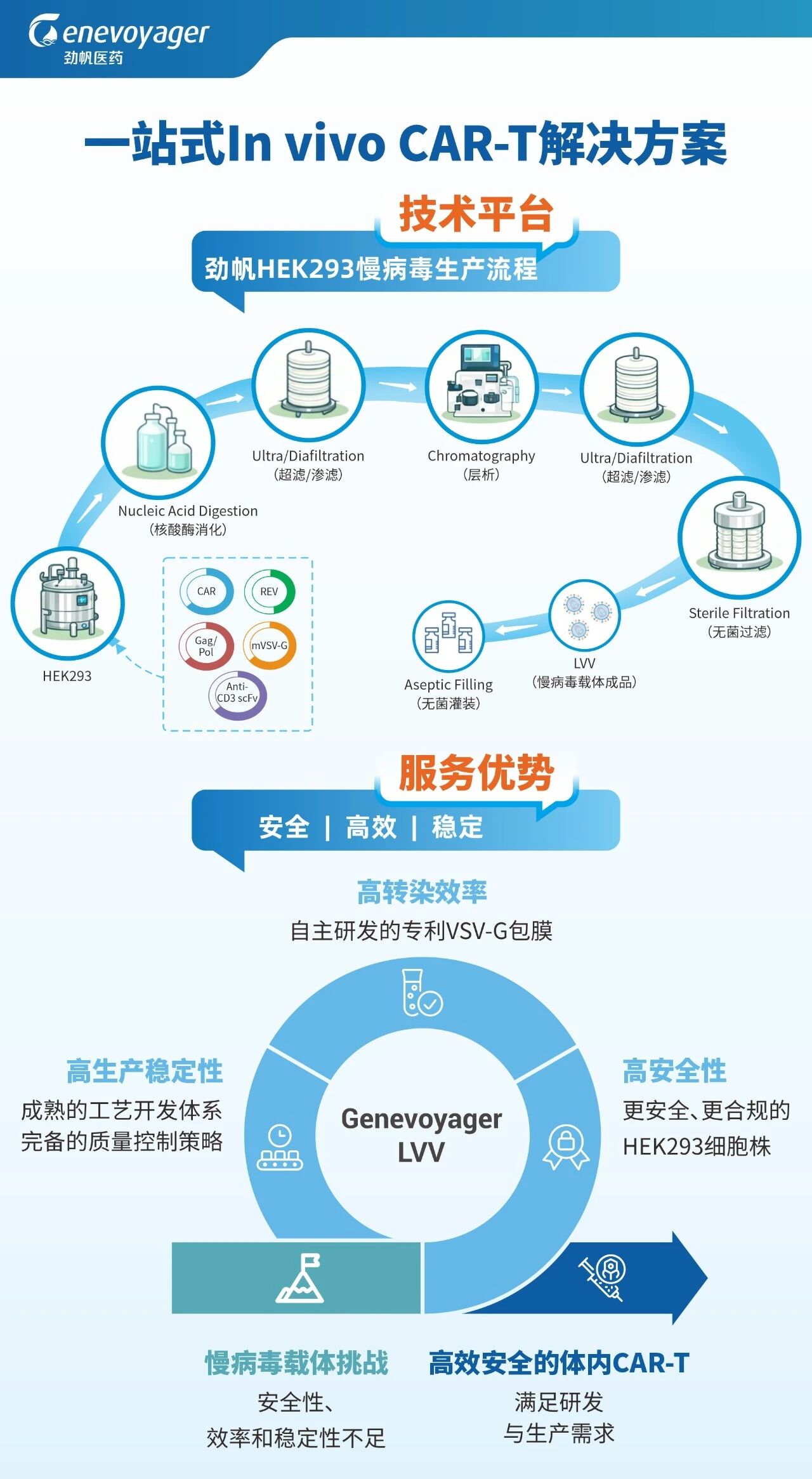
劲帆医药专注于In vivo CAR-T领域慢病毒载体CDMO全流程服务,致力于为全球细胞与基因治疗企业提供从研究级、GMP-like到商业化GMP级的一站式慢病毒开发、生产与质控解决方案。公司依托自主构建的成熟商业化悬浮慢病毒生产平台,具备完善的上游工艺开发、下游纯化、质量研究与分析检测能力,可提供非注册临床样品制备、临床及商业化产品GMP生产、IIT/IND一体化申报、分析检测与技术咨询等全链条服务,满足客户从早期研发到商业化上市的全生命周期需求。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。