2026-05-11
导读
ROS1融合是非小细胞肺癌(NSCLC)中明确的致癌驱动因素,发生率约1%–2%。尽管一代、二代ROS1-TKI显著改善患者预后,但ROS1 G2032R耐药突变、脑转移发生率高以及TRK脱靶导致的中枢神经系统(CNS)毒性三大临床瓶颈,始终制约长期获益。近日,发表于顶刊《Cancer Cell》的研究“JYP0322, a highly selective and brain-penetrant ROS1 inhibitor, overcomes ROS1G2032R resistance mutation in NSCLC: The first-in-human phase 1 trial”公布了新一代大环类ROS1抑制剂JYP0322的重磅数据,该药物凭借精准结构设计实现“强效克服耐药、高脑穿透性、极低神经毒性”三重突破,为ROS1融合阳性晚期NSCLC提供了全新治疗选择。
——核心亮点
● JYP0322是新一代高选择性ROS1抑制剂,可克服ROS1 G2032R耐药突变。
● JYP0322不抑制TRKA/B/C,患者中枢神经系统毒性发生率低。
● 对ROS1靶向药初治非小细胞肺癌患者客观缓解率达95.7%,经治患者达52.6%。
● 血脑屏障穿透性优异(脑脊液/血浆比值0.893),颅内病灶客观缓解率达55.6%。
一、临床需求:ROS1靶向治疗仍存未满足刚需
ROS1作为受体酪氨酸激酶,通过染色体重排形成CD74-ROS1等融合变体,驱动激酶异常活化。一代抑制剂克唑替尼客观缓解率(ORR)仅60-70%,且无法透过血脑屏障,G2032R是最主要耐药突变,临床无有效药物。二代药物洛拉替尼、恩曲替尼、瑞波替尼、他雷替尼颅内活性提升,但仍难以克服G2032R,且因抑制TRKA/B/C导致CNS毒性高达30-50%,头晕、共济失调、味觉障碍频发,严重影响生活质量。
当前已获批药物均无法同时实现广谱覆盖耐药突变、强效入脑、低神经毒性,临床迫切需要新一代高选择性、脑穿透性ROS1抑制剂。
二、药物设计:紧凑大环结构+氰基修饰,实现精准靶向
JYP0322为大环类ROS1抑制剂,核心设计突破体现在两个方面:
1)紧凑大环骨架:可有效规避ROS1 G2032R突变引入精氨酸残基造成的空间位阻,保持对突变体的强效抑制,解决最棘手的耐药机制。
2)吡唑核心氰基(-CN)修饰:与TRKA中Tyr591产生空间位阻,而ROS1对应位点Leu2028体积更小不产生干扰,实现ROS1高选择性,不抑制TRKA,从源头降低神经毒性。
临床前理化与成药性优化显示,JYP0322中枢神经系统多参数优化(MPO)评分4.5,具备优异血脑屏障穿透潜力(图1)。
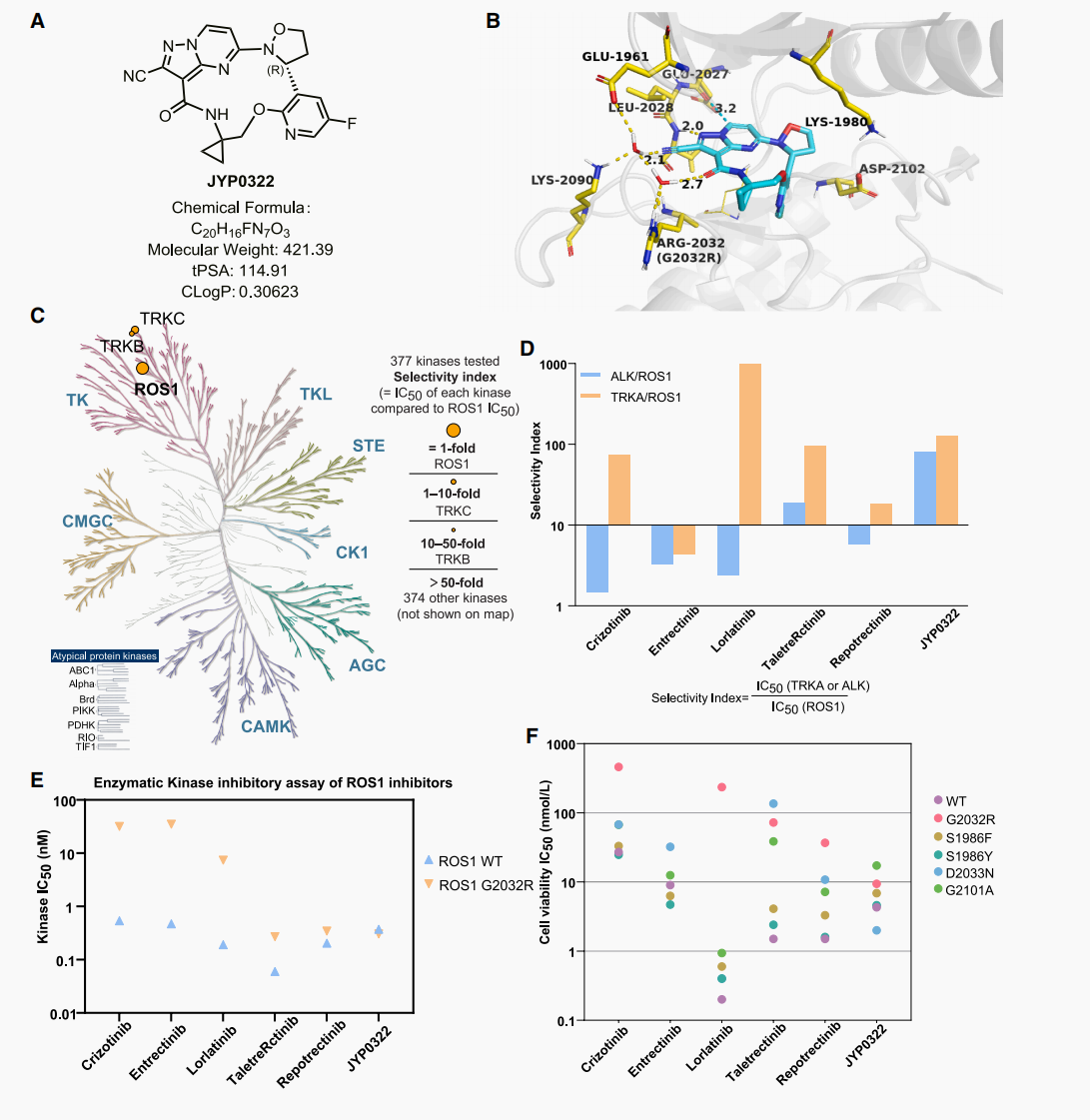
图1 JYP0322的药物设计、生化活性及细胞活性研究
三、临床前核心结果:强效抑制ROS1/WT及G2032R突变,高脑穿透
(一)激酶选择性与细胞活性
JYP0322在377种激酶筛选中表现出极高选择性,对TRKA选择性是ROS1的130倍,对TRKB、TRKC分别为20倍、6倍,对ALK抑制微弱(图1C-D)。生化实验显示,JYP0322对ROS1 G2032R的IC50低至0.3nM,略优于野生型ROS1(IC50=0.37nM),显著优于克唑替尼、恩曲替尼、洛拉替尼(图1E)。在稳定表达CD74-ROS1 G2032R、S1986F/Y、D2033N、G2101A的Ba/F3细胞中,JYP0322均表现出强效增殖抑制活性(图1F)。
(二)体内抗肿瘤疗效
在Ba/F3 CD74-ROS1野生型异种移植模型中,JYP0322剂量依赖性抑制肿瘤生长,5mg/kg BID疗效即与30mg/kg QD克唑替尼相当(图2A)。在SDC4-ROS1 PDX模型中,3mg/kg BID即可实现87.3%肿瘤生长抑制,与10mg/kg QD恩曲替尼相当(图2B)。
在ROS1 G2032R皮下模型中,5mg/kg与15mg/kg剂量组肿瘤生长抑制率分别达81.7%、100.3%,诱导肿瘤消退,疗效优于瑞波替尼与他雷替尼(图2C)。在颅内肿瘤模型中,JYP0322可显著延长小鼠生存期,优于同类药物,且体重下降更轻微(图2D-E)。犬类药代结果显示,脑脊液/血浆游离药物AUC比值达0.893,证实强效脑穿透能力(图2)。
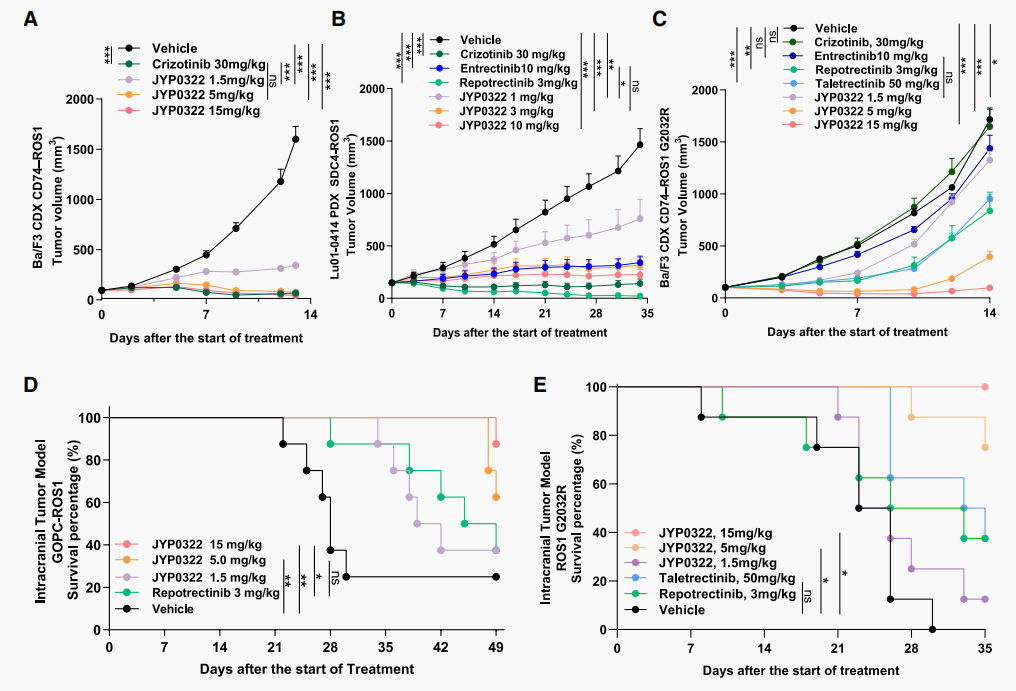
图2 JYP0322的体内抗肿瘤活性与优异血脑屏障穿透能力
四、Ⅰ期临床研究设计与患者基线
本研究为多中心、开放标签、首次人体Ⅰ期试验(NCT06128148),旨在评估JYP0322治疗局部晚期/转移性ROS1融合阳性NSCLC的安全性、药代动力学(PK)与初步疗效。剂量递增采用50mg QD至150mg TID,剂量扩展阶段纳入更多患者。
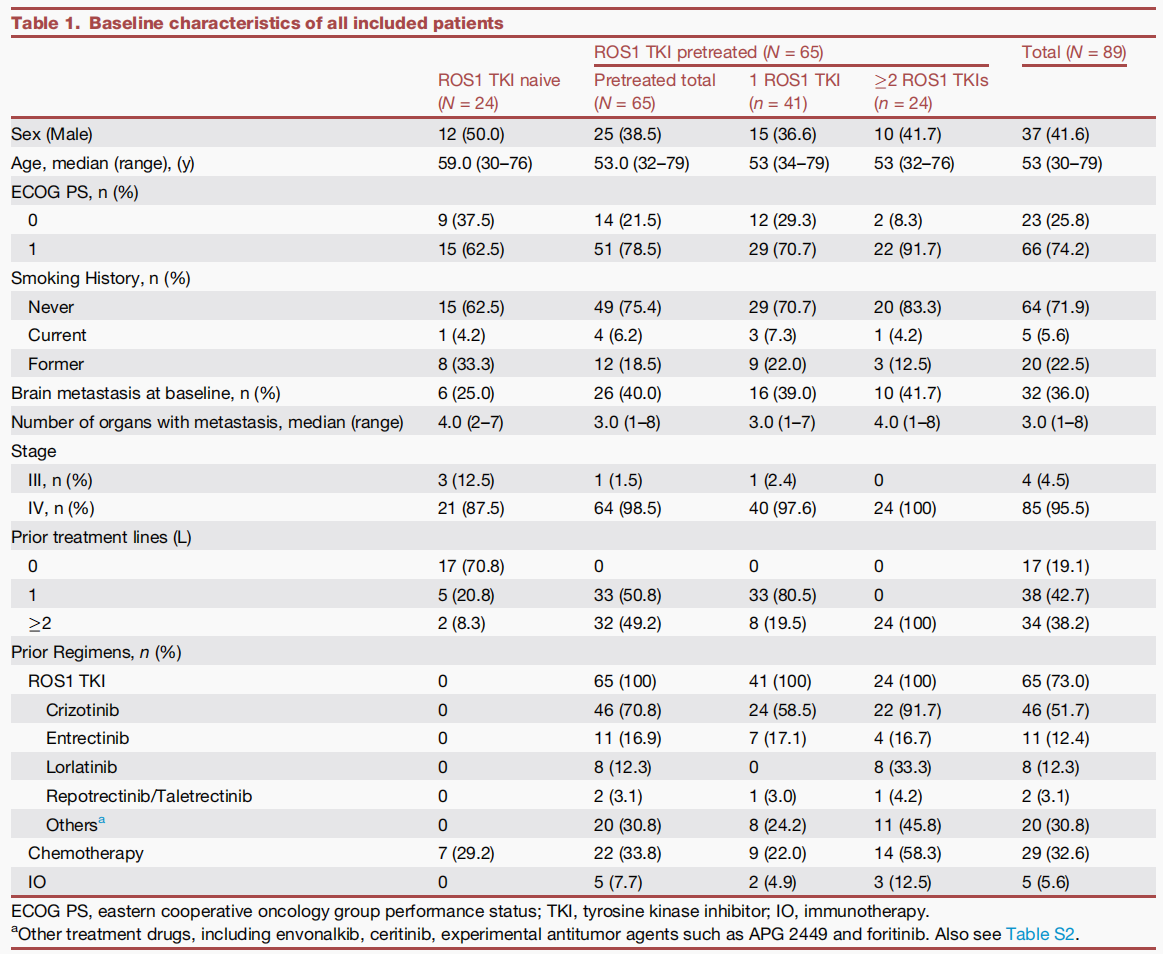
截至2025年4月30日,共筛选128例,入组89例患者,36.0%伴脑转移,73.0%为ROS1-TKI经治,其中24例接受≥2线ROS1-TKI治疗。所有患者ECOG PS 0-1分,基线多伴多器官转移(表1)。
表1 所有入组患者基线临床特征
五、临床核心结果:疗效卓越,覆盖初治、经治、耐药与脑转移
(一)总体抗肿瘤疗效
80例可评估疗效患者中,TKI初治ORR高达95.7%,DCR 100%;TKI经治ORR 52.6%,DCR 77.2%。接受≥2线ROS1-TKI患者ORR仍达57.1%,DCR 71.4%,中位PFS 8.3个月(图4)。
在ROS1 G2032R突变患者(n=9)中,ORR高达77.8%,中位PFS尚未达到;非G2032R经治患者ORR 47.9%,中位PFS 8.1个月。1例G2032R/L1951R共突变患者经克唑替尼治疗失败后,使用JYP0322达到部分缓解(PR)(图5)。
脑转移患者中,颅内可评估人群ORR 55.6%,DCR 88.9%;初治脑转移患者颅内ORR 达100%,经治患者为33.3%(图5)。
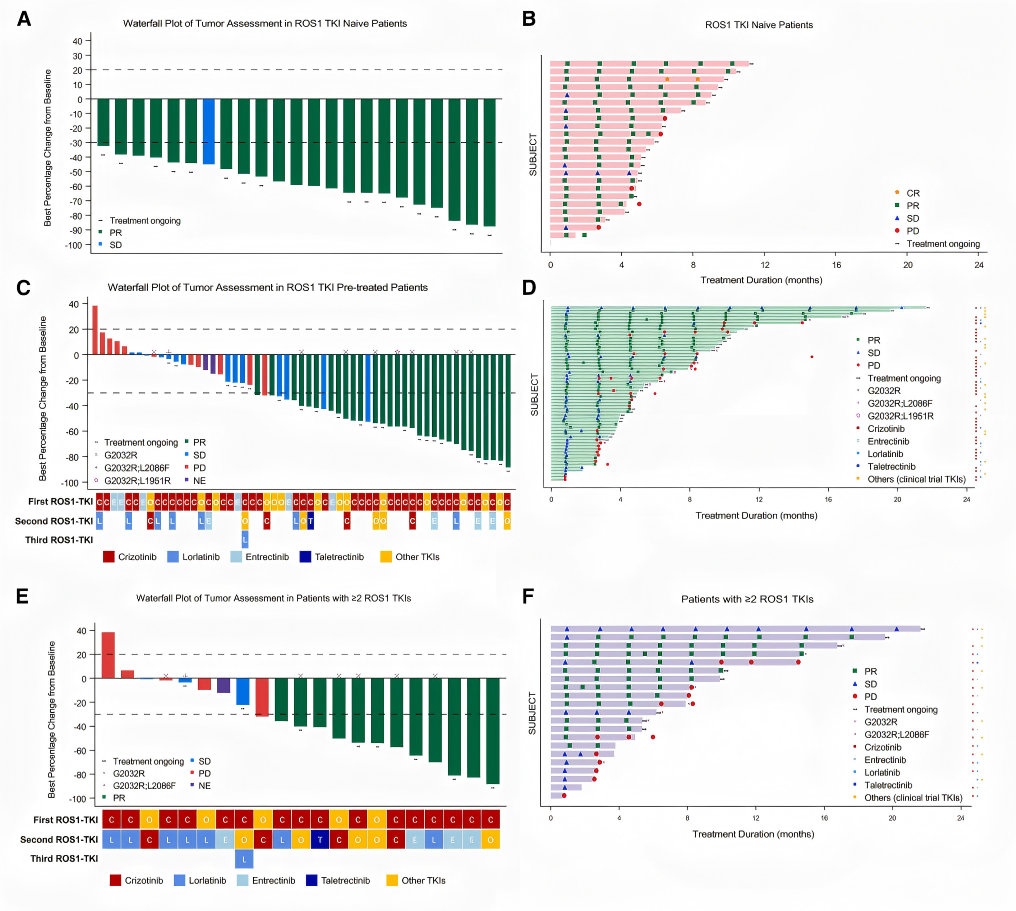
图4 肿瘤基线最佳缓解情况与治疗全程进程
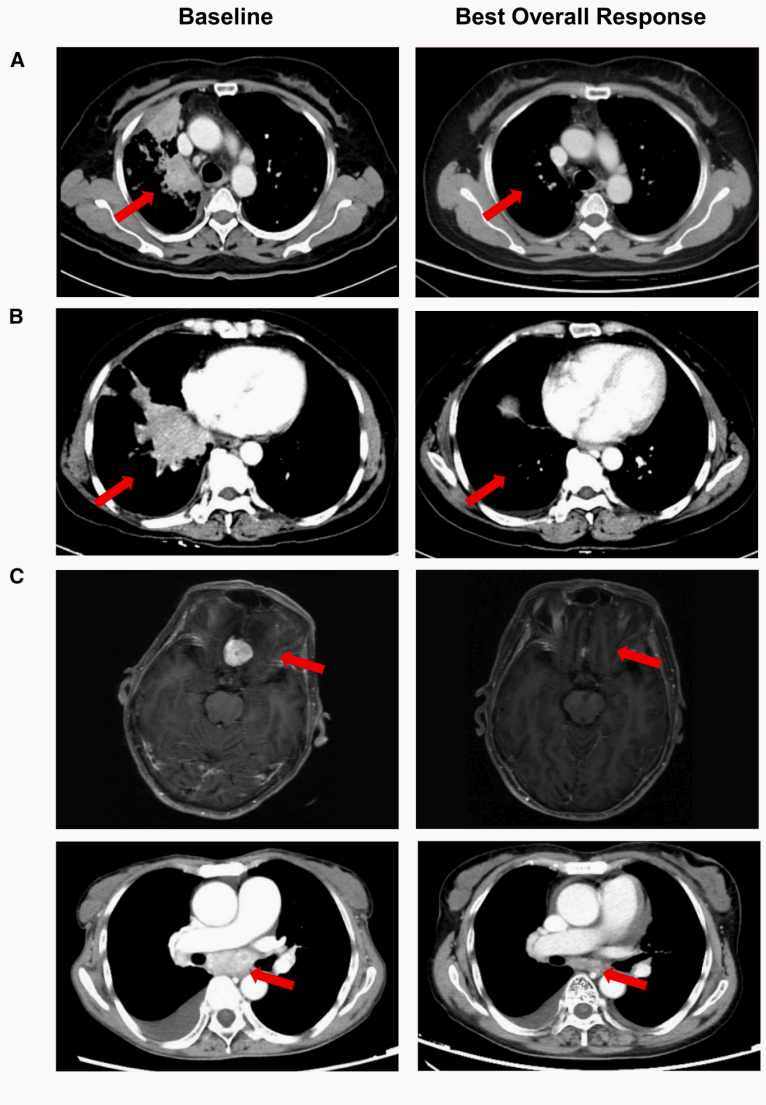
图5 达到部分缓解患者的典型影像学检查图像
(二)安全性数据
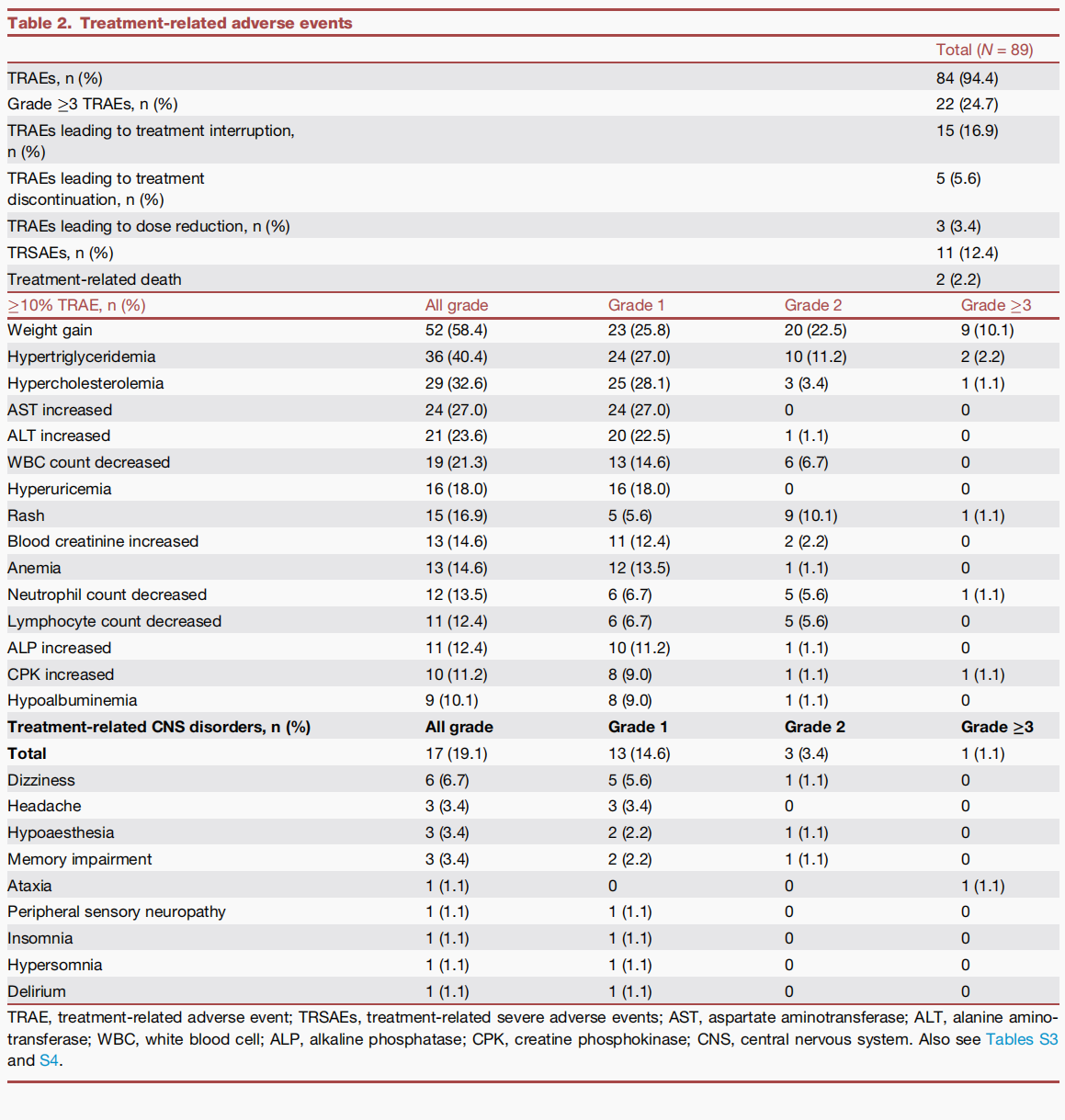
89例患者中,94.4%出现治疗相关不良反应(TRAEs),≥3级TRAEs仅24.7%。因TRAEs停药5.6%,剂量调整3.4%,治疗相关死亡2例(2.2%)。最常见TRAEs为体重增加(58.4%)、高甘油三酯血症(40.4%)、高胆固醇血症(32.6%)、AST升高(27.0%)、ALT升高(23.6%),绝大多数为1-2级,临床可控(表2)。
最具临床价值的是,CNS相关TRAEs发生率极低:头晕6.7%、头痛3.4%、感觉减退3.4%、记忆障碍3.4%,均为1-2级;仅1例3级共济失调,对症治疗后缓解。这一安全性特征显著优于现有二代ROS1抑制剂(CNS毒性23.1-58%)。
表2 治疗相关不良事件
(三)药代动力学特征
JYP0322吸收迅速,Tmax约2-4h。100mg QD及以上剂量稳态暴露即可超过ROS1及G2032R突变体的IC90阈值(图6)。多次给药后蓄积比<2,无明显蓄积。患者脑脊液/游离血浆浓度比1.20,进一步验证优异脑穿透能力。
综合安全性、PK与疗效,研究确定Ⅱ期推荐剂量(RP2D)为150mg BID或150mg TID。
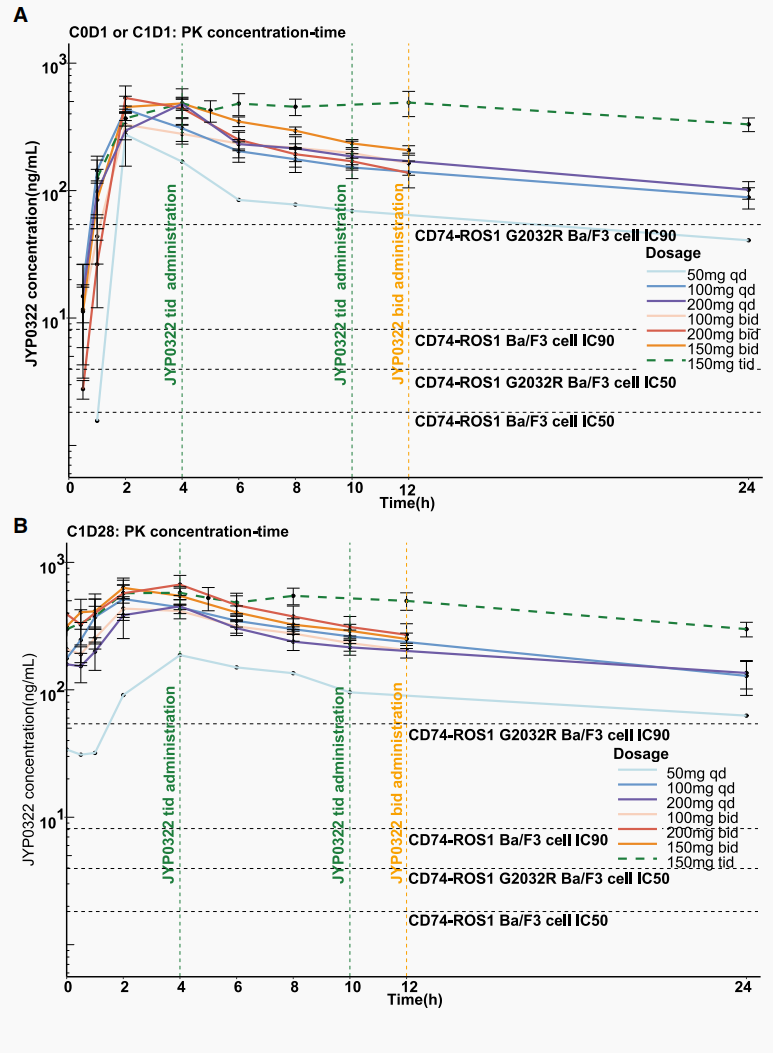
图6 人体多次口服给药后JYP0322平均血浆浓度-时间变化曲线
六、耐药机制探索
研究对26例配对治疗前后样本进行分析,发现JYP0322耐药以ROS1非依赖机制为主,仅2例出现ROS1依赖型耐药,均为L2086F看门突变合并TP53变异。提示旁路通路激活是主要耐药模式,未来联合策略应重点关注此类机制。
七、讨论:JYP0322三大核心突破,重新定义ROS1治疗范式
突破1:强效克服ROS1 G2032R耐药G2032R是ROS1最经典、发生率最高、临床最难治的耐药突变,克唑替尼、恩曲替尼、洛拉替尼均无效。JYP0322凭借紧凑大环结构,突破空间位阻,实现对G2032R的强效抑制,ORR达77.8%,为该类患者提供了首个明确有效的治疗选择。
JYP0322对TRKA选择性>130倍,几乎不抑制TRKA/B/C,神经毒性大幅下降。头晕仅6.7%、头痛3.4%,无明显记忆、睡眠、共济失调等不良反应,安全性显著优于现有二代药物,更适合长期持续治疗。
ROS1阳性患者脑转移发生率高达20-40%,是治疗失败的主要原因之一。JYP0322脑脊液/血浆比值高,颅内ORR达55.6%,初治脑转移患者颅内ORR 100%,实现全身与颅内病灶同步控制。
整体而言,JYP0322在初治、经治、G2032R耐药、脑转移四类难治人群中均表现出优异疗效,同时具备更高安全性,有望成为ROS1融合阳性NSCLC的全新标准治疗。
八、总结与展望
该研究首次系统报道新一代高选择性、脑穿透性ROS1抑制剂JYP0322的临床前与Ⅰ期临床数据,证实该药物具备三大核心优势:强效克服ROS1 G2032R耐药、高血脑屏障穿透、极低CNS神经毒性。在89例ROS1融合阳性晚期NSCLC患者中,JYP0322展现出卓越疗效:初治ORR 95.7%,经治ORR 52.6%,G2032R突变ORR 77.8%,颅内ORR 55.6%,且安全性优异,CNS毒性显著低于同类药物。
JYP0322的成功研发,代表了精准结构设计+高选择性激酶抑制的新一代靶向药开发范式,为解决ROS1耐药、脑转移、神经毒性三大临床难题提供了里程碑式新方案。目前针对经治ROS1阳性患者的Ⅲ期注册临床试验已启动,有望快速改变临床实践。
随着精准医疗与新药研发的持续推进,ROS1融合阳性NSCLC已逐步走向“长期慢病化”。JYP0322作为新一代旗舰药物,将推动领域进入高效、安全、颅内全覆盖的全新治疗时代,为更多患者带来长期生存获益。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。