2026-05-11
导读
近日,国际知名学术期刊《EMBO Molecular Medicine》在线发表了题为“Systemic delivery of AAV-GFM1 corrects COXPD1 molecular alterations in Gfm1R671C/-mice”的最新研究成果。该研究首次利用高度重现人类患者病理特征的Gfm1基因突变小鼠模型,证实通过腺相关病毒(rAAV)介导的系统性基因替代疗法,能够成功逆转小鼠肝脏与中枢神经系统中的深层分子缺陷,为攻克这一致命罕见病带来了切实的新希望。
联合氧化磷酸化缺陷1型(COXPD1)是一类极其凶险的神经肌肉代谢疾病,其核心病因在于核基因GFM1发生了致病性突变。GFM1负责编码线粒体翻译延伸因子G1(EFG1),该因子是维持线粒体能量合成工厂正常运转的关键枢纽。一旦突变导致EFG1“罢工”,患者在新生儿期就会遭遇严重的进行性脑病,部分患儿还会并发急性肝功能衰竭,绝大多数在出生后数日或数月内便不幸夭折。
然而,面对如此迅猛的病情,临床上长期束手无策,仅能依赖姑息支持治疗。为了打破“无药可救”的临床僵局,研究团队开展了从体外细胞到活体动物的系统性基因治疗探索,并在逆转疾病表型上取得了令人振奋的突破。
慢病毒介导的GFM1补充在体外挽救患者细胞功能
在开展动物活体实验前,研究团队首先验证了基因补充的体外疗效。研究人员将携带人类GFM1的慢病毒载体(p305-GFM1LV)转导至三名COXPD1患者的成纤维细胞中。
结果显示,接受基因补充后,细胞内的EFG1表达量不仅大幅恢复,更达到健康对照水平的3至5倍。同时,患者细胞中原本严重受损的呼吸链复合物Ⅰ(CⅠ)和复合物Ⅳ(CⅣ)的酶活性缺陷也得到了显著的实质性纠正。这从概念上直接证明了导入正常基因可逆转疾病细胞的能量代谢危机。
[注:详见论文补充材料Figure EV2,集中展示了患者成纤维细胞在慢病毒转导后EFG1蛋白表达及呼吸链复合物活性的恢复情况]
AAV9靶向肝脏递送显著纠正氧化磷酸化缺陷
针对核心受累器官,研究在精准重现人类病理特征的Gfm1R671C/-突变小鼠中进行了评估。在肝脏靶向策略中,向6周龄小鼠静脉注射搭载肝细胞特异性启动子的AAV9载体(AAV9-hAAT-GFM1)四周后,小鼠肝脏被成功转导。受性别因素影响,雄鼠肝脏的载体拷贝数和转录水平约为雌鼠的三倍,促使雌雄小鼠肝脏线粒体中的EFG1蛋白分别显著提升20.4%和53.6%。
外源性EFG1重启了受损的线粒体翻译机制,使CⅣ亚基(COX1和COX2)稳态水平大幅恢复,并促进了核编码CⅠ亚基(如NDUFA9)的稳定留存。生化分析证实,肝脏中完整组装的CⅠ和CⅣ水平大幅增加,其酶活性近乎完全恢复至野生型健康小鼠水平。
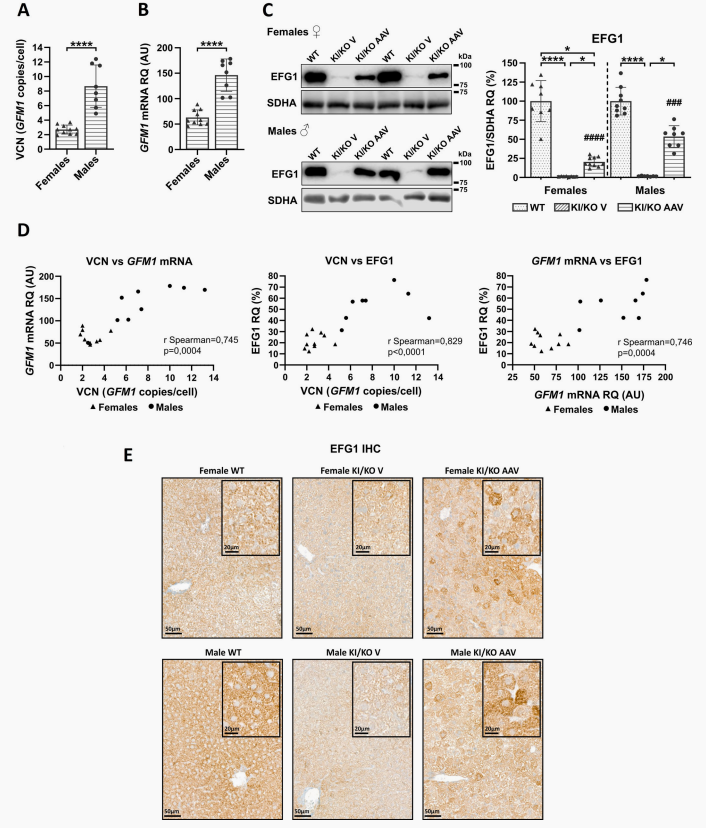
图1 AAV9-hAAT-GFM1载体在Gfm1R671C/-小鼠肝脏中的转导及hGFM1蛋白表达
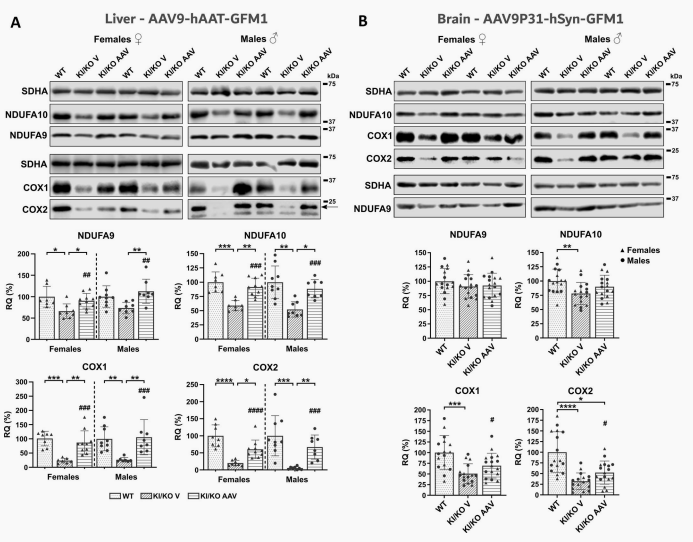
图3 经rAAV治疗的Gfm1R671C/-小鼠肝、脑线粒体中呼吸链复合体Ⅰ、复合体Ⅳ亚基的蛋白表达水平
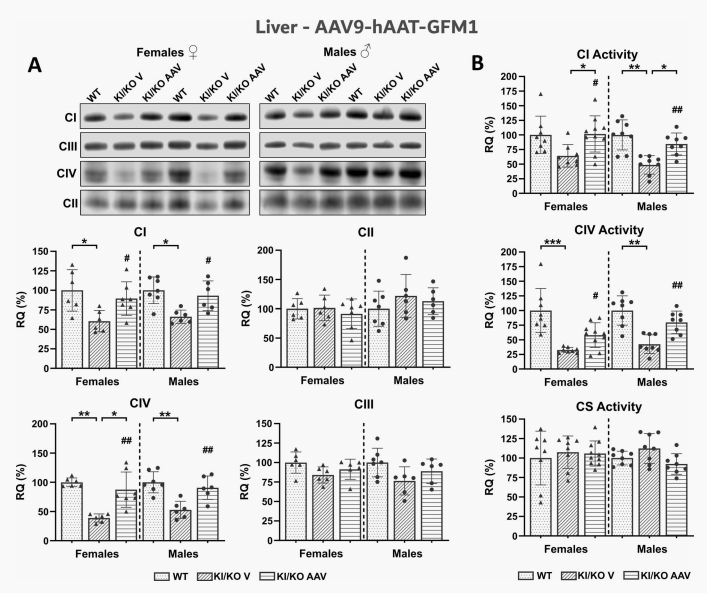
图4 AAV9-hAAT-GFM1对Gfm1R671C/-小鼠肝脏复合型氧化磷酸化功能缺陷的修复作用
图1、图3A及图4,集中展示了AAV9载体在小鼠肝脏的转导效率、OXPHOS蛋白亚基恢复及酶活性的全面纠正。
AAV9P31靶向中枢神经系统改善脑部线粒体酶活性
为应对致死性的新生儿脑病,团队采用具备极强中枢穿透力的AAV9P31衣壳,搭载神经元特异性启动子构建了靶向脑部的载体(AAV9P31-hSyn-GFM1)。
静脉给药四周后,该载体在雌雄小鼠脑部均实现高效且无显著性别差异的转导。小鼠脑部线粒体中枯竭的EFG1蛋白水平显著恢复至正常均值的64.8%,CⅣ核心亚基也出现明显的恢复趋势。高精度组织匀浆分光光度分析显示,接受治疗的小鼠脑部CⅠ和CⅣ酶活性较对照组出现了具显著统计学意义的实质性回升,证实了该策略在逆转脑部能量代谢障碍方面的强大效力。
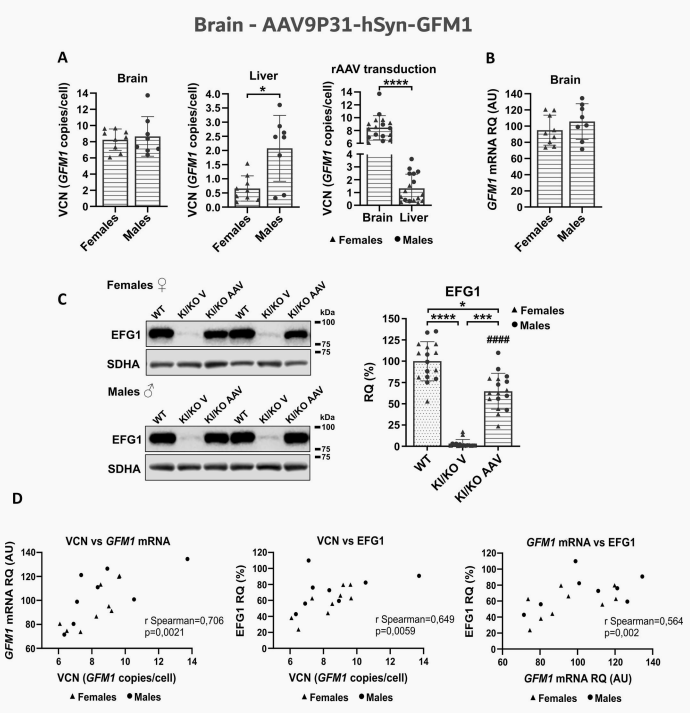
图2 AAV9P31-hSyn-GFM1载体在Gfm1R671C/-小鼠脑组织中的转导及hGFM1蛋白表达
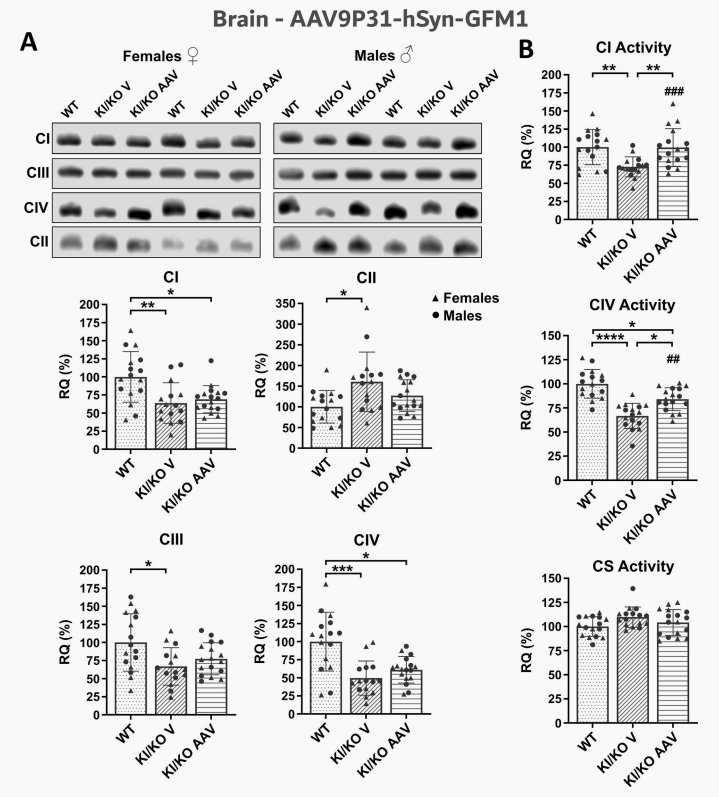
图5 AAV9P31-hSyn-GFM1对Gfm1R671C/-小鼠脑组织复合型氧化磷酸化功能缺陷的修复作用
图2、图3B及图5,集中展示了AAV9P31载体在中枢神经系统中的转导效果及脑部生化活性的显著改善。
基因治疗逆转异常代偿性分子响应
因EFG1耗竭导致翻译长期受阻,突变小鼠肝脏和大脑细胞触发了病理性的代偿响应:线粒体核糖体蛋白(MRPs)水平大幅上升,且线粒体RNA(如Nd4、Cox1 mRNA和12S、16S rRNA)异常扩增与积聚。
接受AAV基因治疗后,随着翻译功能实质性修复,病理代谢压力得以释放。肝脑线粒体中异常升高的MRPs被显著下调,积聚的mtRNA也得到有效回调。这从分子深层证明,基因疗法不仅修补了表面的生化缺陷,更从根源上卸下了疾病强加于细胞的系统性压力。
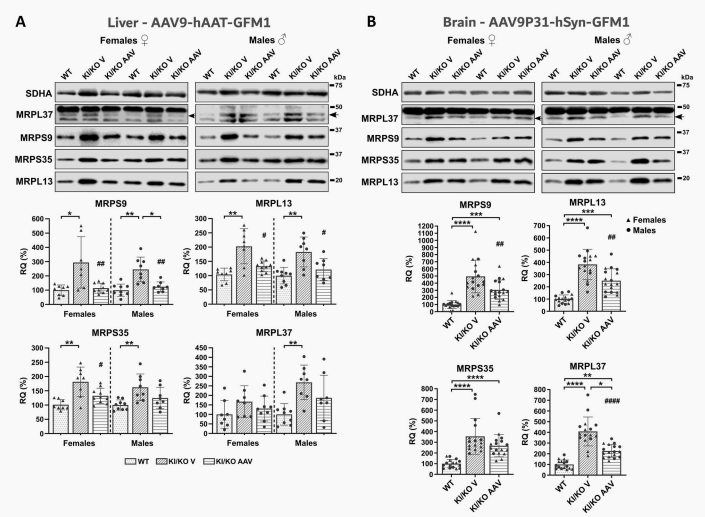
图6 经rAAV治疗的Gfm1R671C/-小鼠肝、脑线粒体中线粒体核糖体蛋白的表达水平
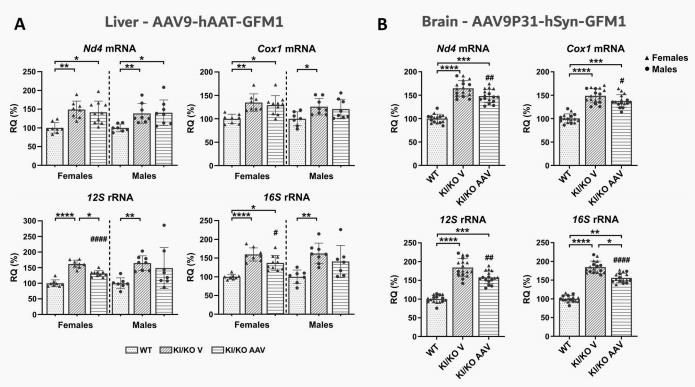
图7 经rAAV治疗的Gfm1R671C/-小鼠肝脏及脑组织中的线粒体RNA水平
表1 纳入本次基因治疗研究的Gfm1R671C/-小鼠线粒体核糖体蛋白与线粒体RNA水平
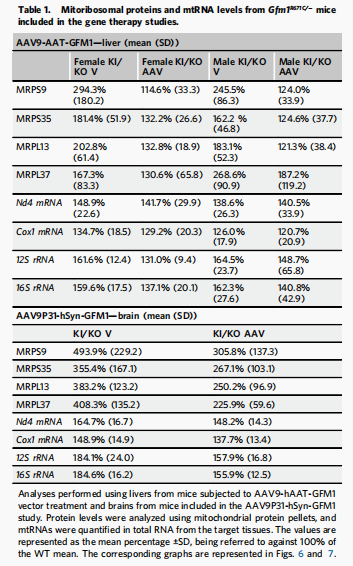
图6、图7及表1,集中展示了AAV基因治疗干预后,针对线粒体核糖体蛋白过表达及mtRNA异常扩增现象的全面平抑与逆转。
总结
该研究首创性证实,通过AAV载体系统性递送GFM1基因,能在短时间内安全、有效地纠正COXPD1小鼠肝脏和中枢神经系统的核心致病缺陷。这打破了该病缺乏有效对因治疗手段的僵局,为这种致死性儿童罕见病提供了首个坚实的体内临床前证据,向彻底治愈迈出了关键一步。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。